题目内容
(2007?连云港)下图中的物质均为初中化学中常见的物质,相互之间存在以下转化关系(某些反应条件已略去).其中A是由四种元素组成的盐,B、G、H、J在常温下均为无色、无味的气体,L为红色粉末状氧化物,I、K为固体单质,白色沉淀F溶于稀硝酸,白色沉淀M不溶于稀硝酸.请回答下列问题: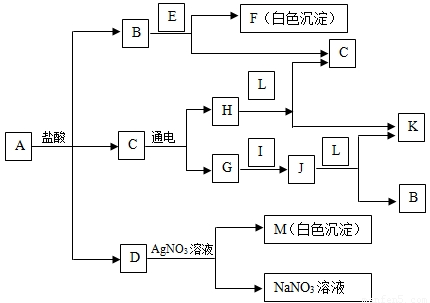
(1)写出下列物质的化学式:C E HI.
(2)写出下列变化的化学方程式:
①A与盐酸反应;
②J与L在高温下反应;
③B与E反应;
④D与AgNO3溶液反应.
【答案】分析:(1)不溶于硝酸的白色沉淀有:硫酸钡和氯化银,D和硝酸银生成的白色沉淀M不溶于硝酸,所以M就是氯化银,D就是氯化钠,H、G均为无色无味的气体,C在通电的条件下会生成H、G,所以C就是水,H会和红色的氧化物反应,所以H就是氢气,G就是氧气,L为红色粉末状氧化物,我们所学过的既是红色,又是金属氧化物的只能是氧化铁,所以L就是氧化铁,氢气和氧化铁反应,生成水和铁,所以C就是水,I是固态单质,氧气和I生成的无色无味的气体J会和氧化铁生成固态单质K,所以I就是碳,J就是一氧化碳,一氧化碳和氧化铁反应生成铁和二氧化碳,所以K就是铁,B就是二氧化碳,二氧化碳和E反应会生成水和可溶于硝酸的白色沉淀,所以E只能是氢氧化钙或氢氧化钡,A和盐酸反应生成氯化钠、水、二氧化碳,A是由四种元素组成的盐,所以A就是碳酸氢钠,将推出的各种物质代入转换关系中进行验证即可.
(2)根据(1)中推出的各个反应的反应物、生成物以及反应条件进行书写化学方程式.
解答:解:(1)D和硝酸银生成的白色沉淀M不溶于硝酸,所以M就是氯化银,D就是氯化钠,H、G均为无色无味的气体,C在通电的条件下会生成H、G,所以C就是水,H会和红色的氧化物反应,所以H就是氢气,G就是氧气,L为红色粉末状氧化物,既是红色又是金属氧化物的只能是氧化铁,所以L就是氧化铁,氢气和氧化铁反应,生成水和铁,所以C就是水,I是固态单质,氧气和I生成的无色无味的气体J会和氧化铁生成固态单质K,所以I就是碳,J就是一氧化碳,一氧化碳和氧化铁反应生成铁和二氧化碳,所以K就是铁,B就是二氧化碳,二氧化碳和E反应会生成水和可溶于硝酸的白色沉淀,所以E只能是氢氧化钙或氢氧化钡,A和盐酸反应生成氯化钠、水、二氧化碳,A是由四种元素组成的盐,所以A就是碳酸氢钠,故答案为:H2O,Ca(OH)2或Ba(OH)2,H2,C,
(2)①碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,故方程式为:NaHCO3+HCl=NaCl+CO2↑+H2O,
②氧化铁和碳在高温的条件下生成铁和二氧化钛,故答案为:Fe2O3+3CO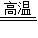 3CO2+2Fe
3CO2+2Fe
③氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,氢氧化钡和二氧化碳反应生成碳酸钡沉淀和水,故答案为:CO2+Ca(OH)2═CaCO3↓+H2O或CO2+Ba(OH)2═BaCO3↓+H2O,
④氯化钠和硝酸银反应生成白色的氯化银沉淀和硝酸钠,故答案为:NaCl+AgNO3═AgCl↓+NaNO3.
点评:在解物质的推断题时,关键是找出题中的“题眼”,而该题的关键点是:白色沉淀M不溶于硝酸.
(2)根据(1)中推出的各个反应的反应物、生成物以及反应条件进行书写化学方程式.
解答:解:(1)D和硝酸银生成的白色沉淀M不溶于硝酸,所以M就是氯化银,D就是氯化钠,H、G均为无色无味的气体,C在通电的条件下会生成H、G,所以C就是水,H会和红色的氧化物反应,所以H就是氢气,G就是氧气,L为红色粉末状氧化物,既是红色又是金属氧化物的只能是氧化铁,所以L就是氧化铁,氢气和氧化铁反应,生成水和铁,所以C就是水,I是固态单质,氧气和I生成的无色无味的气体J会和氧化铁生成固态单质K,所以I就是碳,J就是一氧化碳,一氧化碳和氧化铁反应生成铁和二氧化碳,所以K就是铁,B就是二氧化碳,二氧化碳和E反应会生成水和可溶于硝酸的白色沉淀,所以E只能是氢氧化钙或氢氧化钡,A和盐酸反应生成氯化钠、水、二氧化碳,A是由四种元素组成的盐,所以A就是碳酸氢钠,故答案为:H2O,Ca(OH)2或Ba(OH)2,H2,C,
(2)①碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,故方程式为:NaHCO3+HCl=NaCl+CO2↑+H2O,
②氧化铁和碳在高温的条件下生成铁和二氧化钛,故答案为:Fe2O3+3CO
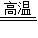 3CO2+2Fe
3CO2+2Fe③氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,氢氧化钡和二氧化碳反应生成碳酸钡沉淀和水,故答案为:CO2+Ca(OH)2═CaCO3↓+H2O或CO2+Ba(OH)2═BaCO3↓+H2O,
④氯化钠和硝酸银反应生成白色的氯化银沉淀和硝酸钠,故答案为:NaCl+AgNO3═AgCl↓+NaNO3.
点评:在解物质的推断题时,关键是找出题中的“题眼”,而该题的关键点是:白色沉淀M不溶于硝酸.

练习册系列答案
相关题目


 (2007?连云港)a、b两物质的溶解度曲线如图1所示,请根据图回答:
(2007?连云港)a、b两物质的溶解度曲线如图1所示,请根据图回答: