题目内容
实验室常用稀盐酸与大理石反应制取二氧化碳气体。
⑴(4分)今有100g36.5﹪的浓盐酸,可稀释成14.6﹪的稀盐酸 ▲ g ,所得稀盐酸中溶质的名称是 ▲ ,配制的步骤是 ▲  ,量取所需水时,应选用的量筒的规格是 ▲ (填序号)① 50ml ② 100ml ③ 200ml
,量取所需水时,应选用的量筒的规格是 ▲ (填序号)① 50ml ② 100ml ③ 200ml
⑵(6分)取上述所配得的稀盐酸50g与12.5g含杂质的大理石恰好完全反应(杂质不参 加反应,也不溶于水)求:(写出计算过程)
加反应,也不溶于水)求:(写出计算过程)
① 生成二氧化碳的质量;
② 所得溶液中溶质的质量分数。(精确的0.1﹪)
⑴可稀释成14.6﹪的稀盐酸 250 g ,所得稀盐酸中溶质的名称是 氯化氢 ,
配制的步骤是 计算、量取、稀释、装瓶贴签 ,应选量筒的规格是200ml 。
⑵解:设反应生成二氧化碳的质量为x,生成氯化钙的质量为y,参加反应的碳酸钙的质量为z
CaCO3+2HCl CaCl2+H2O +CO2↑
100 73 111 44
z 50g×14.6% y x
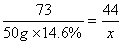 x=4.4g
x=4.4g 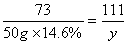 y=11.1g
y=11.1g
 z=10g
z=10g 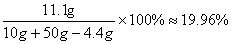
答:反应生成二氧化碳的质量为4.4g,所得溶液的溶质质量分数约为19.96%(或20%)
【其它方法合理即可】

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
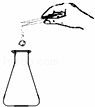
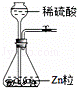
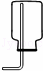
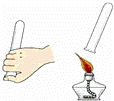
实验室用锌粒和稀硫酸制取氢气的装置及有关实验操作如图所示,其中不正确的是( )
|
| A. |
装入锌粒 | B. |
制取装置 | C. |
收集氢气 | D. |
氢气验纯 |
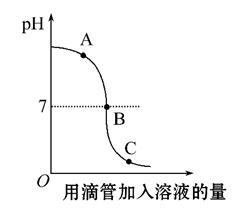
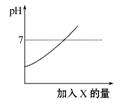 向稀盐酸中逐渐加入试剂X后,溶液的pH变化情况如图所示。试剂X是下列物质中的( )
向稀盐酸中逐渐加入试剂X后,溶液的pH变化情况如图所示。试剂X是下列物质中的( )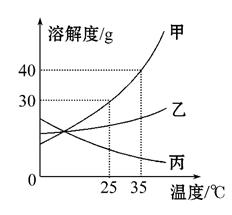
 P+
P+