题目内容
下面是五种粒子的结构示意图:
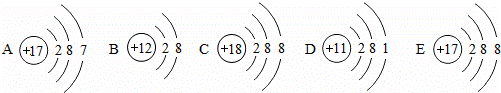
(1)图中粒子共能表示 种元素.A所表示的元素位于元素周期表的第 周期.
(2)图中表示的阳离子是 (用离子符号表示),表示的阴离子是 (用离子符号表示),二者形成的化合物的化学式为 .
| 原子结构示意图与离子结构示意图;元素的概念;化学式的书写及意义;化学符号及其周围数字的意义.. | |
| 专题: | 微观粒子模拟图型. |
| 分析: | 同种元素形成的粒子,质子数相同,原子呈电中性,对阳离子而言,核电荷数>核外电子数.如何找出原子和离子的区别,可以从质子数与核外电子的关系、粒子的带电性等方面加以考虑.原子的核外电子层数表示该元素所处的周期. |
| 解答: | 解:(1)A与E核内质子数相同,表示同一种元素,所以共有4种元素.A原子核外有3个电子层,所以其表示的元素在第3周期.所以答案为:4;3. (2)A、C和D中,核电荷数=核外电子数,表示原子,B中核电荷数>核外电子数,失去2个电子,表示阳离子,形成化合物时常显示+2价,质子数为12,所以该粒子表示镁离子,E中核电荷数<核外电子数,得到1个电子,表示阴离子,形成化合物时常显示﹣1价,质子数为17,所以该粒子表示氯离子,它们形成的化合物为氯化镁.所以答案为:Mg2+;Cl﹣;MgCl2. |
| 点评: | 本题注重基础,考查知识点较多,并且题目难度不很大,对基础知识的掌握有很大帮助,多注重一些规律的记忆和积累. |

 阅读快车系列答案
阅读快车系列答案既要在一充满空气的瓶子中,将其中的氧气除去.又不增加其他气体的成分.下列物质在瓶中燃烧可达到目的是( )
|
| A. | 木炭 | B. | 硫磺 | C. | 铁丝 | D. | 红磷 |
今上半年,云南等五省市持续严重干旱,造成人、畜饮水困难.水是生命之源,应该爱护水资源.下列净化水的方法中发生了化学反应的是( )
|
| A. | 通过蒸馏来净化水 | B. | 通过过滤来净化水 |
|
| C. | 用活性炭来净化水 | D. | 用明矾来净化水 |
在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是( )
| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X | 26 | 2 | 12 |
|
| A. | 该变化的基本反应类型是分解反应 | B. | 反应后物质M的质量为13g |
|
| C. | 反应中N、P的质量比为5:4 | D. | 物质Q可能是该反应的催化剂 |
铁在潮湿的空气里会发生锈蚀,证明氧气一定参加了反应必须要做的实验是( )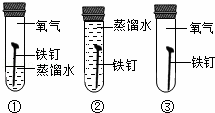
|
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
观察以下化学反应的微观示意图,下列说法不正确的是( )
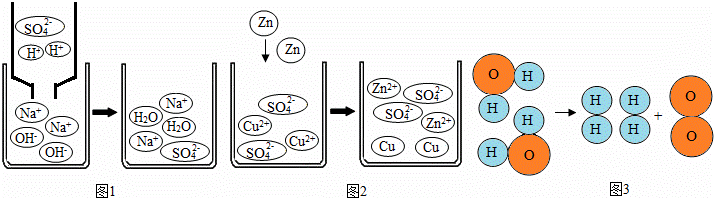
|
| A. | 图1的反应中,微观上是H+和OH﹣生成水分子及Na+和SO42﹣生成Na2SO4分子的过程 |
|
| B. | 图2中的反应,微观上是锌原子和铜离子生成锌离子和铜原子的过程 |
|
| C. | 图3中的反应,微观上是分子的破裂,原子的重新组合生成新分子过程 |
|
| D. | 上述所涉及的化学反应基本类型有复分解反应、置换反应、分解反应 |
小明把过量锌粒加入有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体.在反应过程中,溶液的温度也先随之升高,最后下降到室温.于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”.测得实验数据如下:
某金属与同体积盐酸溶液反应实验数据表
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10mL | 60mL |
| 10% | 20℃ | 19mL | 118mL |
| 15% | 20℃ | 28mL | 175mL |
| 5% | 35℃ | 28mL | 60mL |
| 10% | 35℃ | 72mL | 118mL |
| 15% | 35℃ | 103mL | 175mL |
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有 、 .
(2)可以通过比较 实验数据来确定金属和酸反应的快慢.
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢.请分析原因. .
 糖与果糖 D.甘氨酸与硝基乙烷(C2H5NO2)
糖与果糖 D.甘氨酸与硝基乙烷(C2H5NO2)