题目内容
3.天燃气是我市即将引进优质燃料,它热值大,污染小,写出有关的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.将银白色的铝条放入蓝色的硫酸铜溶液中,过一会取出发现铁钉表面附着一红色固体,有关反应的化学方程式是2Al+3CuSO4=Al2(SO4)3+3Cu.
分析 根据天然气的主要成分是甲烷,甲烷燃烧生成水和二氧化碳解答;首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:天然气的主要成分是甲烷,甲烷燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
铝的活动性比铜强,将铝丝插入到蓝色硫酸铜溶液中,铝能与硫酸铜反应生成硫酸铝和铜,可观察到铝丝表面出现红色固体,溶液由蓝色逐渐变为无色,反应的化学方程式为:2Al+3CuSO4=Al2(SO4)3+3Cu.
故答案为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 蓝 2Al+3CuSO4=Al2(SO4)3+3Cu.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
18.围绕一瓶氢氧化钠固体是否变质的问题,同学们展开探究活动.查阅资料:氢氧化钠变质生成碳酸钠;碳酸钠溶液的PH大于7.
(1)甲同学用酚酞试液检验氢氧化钠是否变质.你认为他能否成功不能,理由是:碳酸钠的水溶液呈碱性也能使酚酞试液变红
(2)乙同学取少量固体于试管中,滴加某种试剂,有大量气泡产生,由此证明氢氧化钠已经变质.你认为所加试剂为:稀盐酸.
(3)丙同学欲证明变质的固体中尚存有氢氧化钠,请帮助他完成以下探究方案:
(1)甲同学用酚酞试液检验氢氧化钠是否变质.你认为他能否成功不能,理由是:碳酸钠的水溶液呈碱性也能使酚酞试液变红
(2)乙同学取少量固体于试管中,滴加某种试剂,有大量气泡产生,由此证明氢氧化钠已经变质.你认为所加试剂为:稀盐酸.
(3)丙同学欲证明变质的固体中尚存有氢氧化钠,请帮助他完成以下探究方案:
| 探究目标 | 探究步骤 | 探究现象 |
| 目的:证明固体中存在碳酸钠 | 取少量固体溶于水,向其中滴加足量的氯化钙溶液. | 产生白色沉淀 |
| 证明固体中存在氢氧化钠 | 向上述所得溶液中滴酚酞试液 | 酚酞试液变红 |
15.下列有关资源和能源的叙述正确的是( )
| A. | 核能、太阳能等新型能源的使用可以部分解决化石燃料面临耗尽的问题 | |
| B. | 煤隔绝空气加强热可以分解成焦炭、煤焦油、汽油等物质 | |
| C. | 地球表面约96.5%被水覆盖 | |
| D. | 地壳和海洋中的金属资源储量无限,而且可再生 |
12.某铜的合金中另含锌、镁中的某种金属、为了确认其成分进行如下实验:取该合金样品10.00g放入烧杯,然后将56.00g某稀硫酸平均分四次加入其中,每次充分反应后烧杯内剩余物质的质量记录如下、把第4次加入稀硫酸后所剩的固体物质滤出.经洗涤、干燥后称重为6.10g.请回答下列问题:
(1)合金中铜与另一金属的质量比为61:39,实验中生成H2的总质量为0.12g
(2)通过计算,确定该稀硫酸中溶质的质量分数和另一种金属是什么?
| 序号 | 1 | 2 | 3 | 4 |
| 加稀硫酸的质量/g | 14.00 | 14.00 | 14.00 | 14.00 |
| 剩余物质的质量/g | 23.96 | 37.92 | 51.88 | 65.88 |
(2)通过计算,确定该稀硫酸中溶质的质量分数和另一种金属是什么?
6.下列说法中正确的是( )
| A. | 铁矿石用于炼铁是因为铁矿石中含有大量的单质铁 | |
| B. | 铁在金属活动性顺序中排在氢的前面,所以可把稀硫酸中的氢气置换出来 | |
| C. | 生铁是含杂质很多的铁合金 | |
| D. | 盛水的铁桶最早生锈的部位是水面附近 |
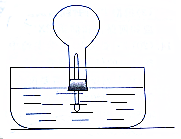 如图所示,如果挤压胶头滴管,并取下胶帽,便可发现喷泉现象,请说出水槽中液体(与胶头滴管内液体相同)和烧瓶中气体的可能成分(至少写出两种情况),并分析他们是利用了物质的什么性质,发生什么变化,如果是化学变化,请写出化学方程式.
如图所示,如果挤压胶头滴管,并取下胶帽,便可发现喷泉现象,请说出水槽中液体(与胶头滴管内液体相同)和烧瓶中气体的可能成分(至少写出两种情况),并分析他们是利用了物质的什么性质,发生什么变化,如果是化学变化,请写出化学方程式.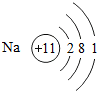 ,钠离子
,钠离子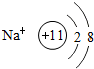 .指出钠原子和钠离子在结构上的相同点和不同点质子数相同、核外电子数不同.
.指出钠原子和钠离子在结构上的相同点和不同点质子数相同、核外电子数不同.