题目内容
9.实验室配制500g溶质的质量分数为0,5%的KMnO4溶液,用于对种子进行消毒,现准备如下实验用品,请回答下列问题: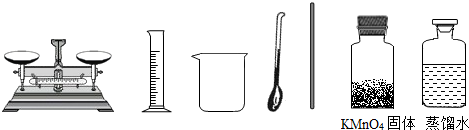
(1)称量KMnO4固体时,药品应放在托盘天平左(填“左”或“右”)盘的纸片上,天平上的游码位置应是图中的C(填字母).
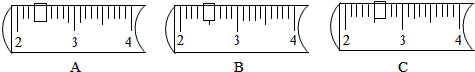
(2)量取所需水时,除上述准备的实验用品外,还需要的一种仪器是胶头滴管(填名称).若仰视读数,则所配制的溶液,其溶质的质量分数会偏小(填“偏大”、“偏小”或“不变”).
分析 (1)根据使用托盘天平称取固体物质质量的操作方法:左物右码、砝码的选用、游码的调整分析解答;
(2)根据量筒的使用注意事项解答;仰视读数偏小,实际量取的水体积较多,会造成配制溶液的溶质质量分数会偏大.
解答 解:(1)称取固体物质,放在烧杯内根据“左物右码”的原则放在左边托盘内进行称取,KMnO4质量为500g×0.5%=2.5g;所以选择游码应移动至2.5g处,游码左侧示数为游码质量,图中A表示2.3g、B表示2.4g、C表示2.5g;
(2)量取蒸馏水时,将蒸馏水注入量筒,待液面接近量取体积对应刻度线时,改用胶头滴管滴加蒸馏水至刻度线;读数时视线应与凹液面的最低处保持水平;仰视读数偏小,实际量取的水体积偏多,会造成配制溶液的溶质质量分数会偏小.
答案:(1)左;C;(2)胶头滴管;偏小.
点评 本题较细致的考查了天平的使用和溶液配制的误差分析等知识,能结合溶质的质量分数正确分析错误操作引起的后果是解答的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
19.兴趣小组同学在实验室处理废液时,将一瓶已有结块的熟石灰取样,加入含有盐酸的废液中,发现废液中产生大量的气泡.他们进一步了解熟石灰样品变质的程度进行以下探究活动.
【探究活动一】检测熟石灰样品是否完全变质
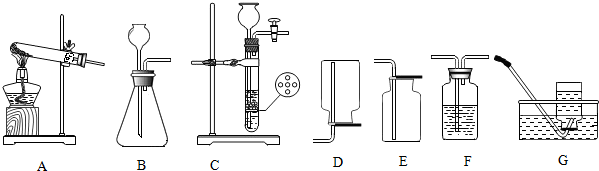
【探究活动二】测定变质的熟石灰样品中碳酸钙的质量分数利用如图所示装置和试剂进行实验(铁架台略去,装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的),称取5g的样品,通过测定样品和稀盐酸
反应产生的气体的质量,计算碳酸钙的质量分数.
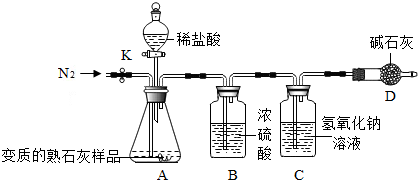
【实验步骤】
①按图连接装置,并检查装置的气密性;
②如图连接装置(除C、D外)并加入5.00g的样品(称量时使用电子天平);
③称量并记录装置C的总质量为200.00g(称量时注意封闭C的两端);
④打开弹簧夹K,鼓入N2约1分钟;
⑤接入装置C、D,关闭弹簧夹K,装置A中加入稀盐酸,至不再产生气泡为止;
⑥重复步骤④操作,称量,装置C的质量为200.88g(称量时注意封闭C的两端);
⑦计算.
回答下列相关问题:
(1)写出A中产生气体的反应化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)装置B中浓硫酸的作用是吸收水分;已知碱石灰的主要成分是CaO和NaOH,则装置D的作用是防止空气中的CO2进入C装置中.
(3)步骤⑤中加入稀盐酸,至不再产生气泡为止,其目的是使得CaCO3完全反应;
(4)步骤⑥中装置C的质量不再增加,说明CO2被NaOH完全吸收,写出装置C中反应的化学方程式:CO2+2NaOH═Na2CO3+H2O.
(5)依题意可得CO2气体的质量为0.88gg,样品中碳酸钙的质量为2gg.测定变质的熟石灰样品中碳酸钙的质量分数=40%.
(6)下列操作会导致测量结果偏低的是D(填序号).
A.省略装置B B.没有进行步骤④的操作C.鼓入N2时间较长 D.步骤⑥没有重复步骤④的操作.
【探究活动一】检测熟石灰样品是否完全变质
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,加水溶解,往上层溶液中滴加无色酚酞 | 溶液显红色 | 变质的熟石灰中仍含氢氧化钙 |
反应产生的气体的质量,计算碳酸钙的质量分数.

【实验步骤】
①按图连接装置,并检查装置的气密性;
②如图连接装置(除C、D外)并加入5.00g的样品(称量时使用电子天平);
③称量并记录装置C的总质量为200.00g(称量时注意封闭C的两端);
④打开弹簧夹K,鼓入N2约1分钟;
⑤接入装置C、D,关闭弹簧夹K,装置A中加入稀盐酸,至不再产生气泡为止;
⑥重复步骤④操作,称量,装置C的质量为200.88g(称量时注意封闭C的两端);
⑦计算.
回答下列相关问题:
(1)写出A中产生气体的反应化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)装置B中浓硫酸的作用是吸收水分;已知碱石灰的主要成分是CaO和NaOH,则装置D的作用是防止空气中的CO2进入C装置中.
(3)步骤⑤中加入稀盐酸,至不再产生气泡为止,其目的是使得CaCO3完全反应;
(4)步骤⑥中装置C的质量不再增加,说明CO2被NaOH完全吸收,写出装置C中反应的化学方程式:CO2+2NaOH═Na2CO3+H2O.
(5)依题意可得CO2气体的质量为0.88gg,样品中碳酸钙的质量为2gg.测定变质的熟石灰样品中碳酸钙的质量分数=40%.
(6)下列操作会导致测量结果偏低的是D(填序号).
A.省略装置B B.没有进行步骤④的操作C.鼓入N2时间较长 D.步骤⑥没有重复步骤④的操作.
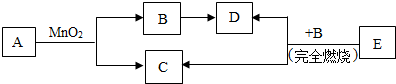
4.某无色气体可能含有CH4、CO、H2中的一种或几种,依次进行下列实验(假设每步反应或吸收均完全)①无色气体在足量氧气中燃烧;②燃烧生成的气体通过盛有浓硫酸的洗气瓶,装置增重3.6g;③再将剩余气体通过盛有NaOH溶液的洗气瓶,装置增重4.4g;下列推断正确的是( )
| A. | 该气体可能只含有CO、H2 | B. | 该气体可能只含有CH4、CO | ||
| C. | 该气体一定只含有CH4 | D. | 该气体一定只含有CH4、H2 |
14.下列实验操作不能达到实验目的是( )
| 选项 | 实验目的 | 主要操作 |
| A | 用自来水制取蒸馏水 | 加热沸腾,水蒸气冷凝 |
| B | 区别化纤与羊毛面料 | 分别取样点燃,闻气味 |
| C | 除去氨气中混有的水蒸气 | 气体通入盛有浓硫酸的洗气瓶中 |
| D | 探究酒精中是否含有碳元素 | 将燃烧产物通入澄清石灰水中 |
| A. | A | B. | B | C. | C | D. | D |
15.下列4个坐标图分别表示4个实验过程中某些量的变化,其中正确的是( )
| A. |  向盐酸中加入水 | B. | 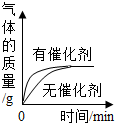 10mL5%的H2O2溶液分解 | ||
| C. | 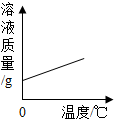 将饱和石灰水升温 | D. | 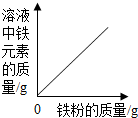 向一定量的稀盐酸中加入铁粉 |
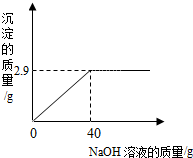 某同学测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取30g该溶液,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液.生成沉淀的质量与所用氢氧化钠溶液的质量关系如图所示.反应方程式为:MgSO4+2NaOH=Na2SO4+Mg(OH)2↓
某同学测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取30g该溶液,向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液.生成沉淀的质量与所用氢氧化钠溶液的质量关系如图所示.反应方程式为:MgSO4+2NaOH=Na2SO4+Mg(OH)2↓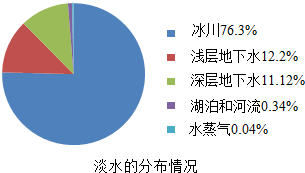 地球上水的分布是:海洋咸水97%,淡水3%,而淡水的分布又如图所示,回答:
地球上水的分布是:海洋咸水97%,淡水3%,而淡水的分布又如图所示,回答: