题目内容
某化学兴趣小组的同学做完“大理石和稀盐酸制取二氧化碳的实验”后,将反应后锥形瓶中残留的废液过滤,并对滤液进行探究(已知大理石中所含杂质既不溶于水,也不与酸反应)。
【提出问题】滤液中所含溶质是什么?
【查阅资料】氯化钙溶液呈中性
【猜想与假设】
猜想1:滤液中的溶质可能是CaCl2和CaCO3
猜想2:滤液中的溶质只有CaCl2
猜想3:滤液中的溶质是 ▲
【讨论与交流】
小明认为猜想1无需验证就知道是错误的,他的理由是 ▲ 。
【实验与结论】
(1)小亮同学为验证猜想2,取少量滤液装入试管中,然后滴入酚酞溶液,发现酚酞溶液不变色,于是小亮认为猜想2正确。你认为他的结论
▲ (填“正确”或“错误”),理由是 ▲ 。
(2)小美为验证猜想3,用洁净干燥的玻璃棒蘸取该滤液滴到湿润的pH试纸上,测得pH=4,她认为猜想3正确。对她的操作方法、测量结果及结论的评价,正确的是 ▲ 。
A.方法不正确,结果偏小,结论正确
B.方法正确,结果偏大,结论不正确
C.方法不正确,结果偏大,结论正确
D.方法正确,结果偏小,结论不正确
(3)小丽选择了其他几种不同类别的物质来验证猜想3,也得出了结论,可供选择的试剂有:石蕊溶液、铜片、镁条、氧化钙、氧化铁、氢氧化钠、氢氧化铜、碳酸钠溶液、硝酸银溶液
请完成下表:
| 方案 | 试剂类别 | 选用试剂 | 实验现象 | 结论 |
| A | 指示剂 | 石蕊溶液 | 溶液变红 | 猜想3 正确 |
| B | 金属单质 | ▲ | 固体表面产生气泡 | |
| C | 金属氧化物 | 氧化铁 | ▲ | |
| D | ▲ | 氢氧化铜 | 固体溶解,溶液变成蓝色 | |
| E | 盐 | 硝酸银溶液 | 产生白色沉淀 |
【反思与评价】上述方案有错误及错误的原因是 ▲ (填写错误方案的序号,并解释其错误的原因)。
【拓展与延伸】
若猜想3成立,小丽认为无需另加试剂,只要对滤液进行 ▲ 操作即可除去杂质,从滤液中得到CaCl2固体。
(4)小丽同学取了100g 滤液,逐滴加入溶质质量分数为10.0%的Na2CO3溶液。反应过程中加入的Na2CO3溶液的质量与溶液pH的关系如下图所示。
试回答下列问题:
① 写出首先发生的反应的化学方程式 ▲ ;
② a点对应的溶液中溶质为 ▲ ;
③ 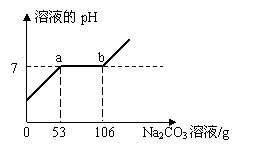 恰好完全反应时所得溶液中溶质的质量分数为 ▲ 。(写出计算过程,结果精确到0.1%)
恰好完全反应时所得溶液中溶质的质量分数为 ▲ 。(写出计算过程,结果精确到0.1%)
【猜想与假设】
CaCl2和HCl
【讨论与交流】
CaCO3难溶于水
【实验与结论】
(1)错误 溶液中的溶质是CaCl2和HCl时,滴加酚酞溶液也不变色。
(2)C;
(3)镁; 固体溶解,溶液变成棕黄色; 碱; E错误,因为若只有CaCl2时,加硝酸银溶液也会产生白色沉淀。
【拓展与应用】
蒸发
(4)① Na2CO3+2HCl=2NaCl+H2O+CO2↑(2分)
② NaCl和CaCl2(或氯化钠和氯化钙);
③ 5.9%(3分)

 导学教程高中新课标系列答案
导学教程高中新课标系列答案