题目内容
复分解反应的定义可以用字母AB+CD=AD+CB来表示.某化学兴趣小组探究稀盐酸与以下四种物质是否能发生复分解反应:
| NaCl溶液 | K2CO3溶液 | AgNO3溶液 | NaOH溶液 |
(1)甲同学提出稀盐酸与NaCl溶液是否发生复分解反应?乙同学认为不反应,因为这两种化合物互相交换成分,所得的物质是一样的.你 (填“同意”或“不同意”)乙同学的看法.
(2)甲乙设计了以下三个实验,请你在空白处填写相关内容:
| 实验操作 | 实验现象 | 实验结论 | |
| 实验1 | 在K2CO3溶液中加入稀盐酸 |
| 稀盐酸与K2CO3溶液发生了复分解反应 |
| 实验2 | 在AgNO3溶液中加入稀盐酸 | 有白色沉淀生成 |
|
| 实验3 | 在NaOH溶液中加入稀盐酸 | 没有明显现象 | 甲乙同学:不发生反应 |
(3)写出实验2的化学方程式: .
(4)在实验3中,甲乙两同学因为观察到没有明显的实验现象,故判断该反应不能进行,你 (填“同意”或“不同意”)他们的看法,若不同意,请设计实验证明该反应能发生.可用试剂:NaOH溶液、稀盐酸、石蕊试液.
| 实验内容与操作 | 实验现象 | 实验结论 |
| 复分解反应及其发生的条件;书写化学方程式、文字表达式、电离方程式. | |||||||||||||||||
| 专题: | 化学反应的基本类型和能量变化. | ||||||||||||||||
| 分析: | (1)根据复分解反应的条件回答; (2) 实验一:根据稀盐酸与K2CO3溶液反应有气泡生成解答; 实验二:根据稀盐酸与AgNO3溶液反应有沉淀生成解答; (3)根据稀盐酸与AgNO3溶液反应生成氯化银沉淀和硝酸,写出反应的方程式; (4)稀盐酸显酸性,能使石蕊试液变红色;氯化钠溶液显中性,不能使酚酞试液变色;NaOH溶液显碱性,能使石蕊试液变蓝色. | ||||||||||||||||
| 解答: | 解: (1)不是任意两种化合物都能发生复分解反应,必须有一定的条件复分解反应才能发生,这里的条件是有气体或水或沉淀生成;故同意; (2) 实验一:稀盐酸与K2CO3溶液反应,生成氯化钾、二氧化碳和水,符合发生复分解反应的条件; 实验二:稀盐酸与AgNO3溶液反应,生成氯化银沉淀和硝酸,符合发生复分解反应的条件; (3)稀盐酸与AgNO3溶液反应生成氯化银沉淀和硝酸,反应的方程式为:HCl+AgNO3 =HNO3 +AgCl↓ (4)氢氧化钠溶液和稀盐酸生成氯化钠和水,符合发生复分解反应的条件,故不同意; 实验操作:向稀盐酸中滴加几石蕊试液,再滴加氢氧化钠溶液; 实验现象:溶液由红 实验结论:盐酸与氢氧化钠发生了化学反应. 答案: (1)同意 (2)
(3)HCl+AgNO3 =HNO3 +AgCl↓ (4)不同意 实验操作:向稀盐酸中滴加几滴石蕊试液,再滴加氢氧化钠溶液; 实验现象:溶液由红色变成紫色; 实验结论:盐酸与氢氧化钠发生了化学反应. | ||||||||||||||||
| 点评: | 判断物质能否反应的关键就是找物质中解离成的离子重新结合生成水或气体或沉淀时,物质就能发生复分解反应. |

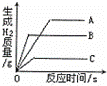
将质量相等的A,B,C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是(已知:A,B,C在生成物中均为+2价)( )
|
| A. | 放出H2的质量是A>B>C | B. | 金属活动性顺序A>B>C |
|
| C. | 相对原子质量是A>B>C | D. | 反应速率最大的是A |
对物质进行归类整理是化学学习的一种重要方法,下列归类关系不相符的是( )
|
| A. | 空气、海水﹣﹣纯净物 | B. | 白磷、红磷﹣﹣可燃物 |
|
| C. | 不锈钢、铜﹣﹣金属材料 | D. | 合成橡胶、塑料﹣﹣有机合成材料 |
 色变成紫色;
色变成紫色;
 所选用的净化方法按净化过程排序(填序号) .
所选用的净化方法按净化过程排序(填序号) .