题目内容
6.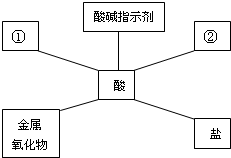 构建知识网络能帮助我们理解知识间的内在联系.请分析如图所示知识网络图,回答有关问题.
构建知识网络能帮助我们理解知识间的内在联系.请分析如图所示知识网络图,回答有关问题.(1)①中填写活泼金属,②中填写碱.
(2)上图中“金属氧化物”若为氧化铁,请你写出稀盐酸与氧化铁反应的化学方程式Fe2O3+6HCl═2FeCl3+3H2O.
(3)使用浓硫酸时要十分小心,浓硫酸有强烈的腐蚀性所以,不要将浓硫酸沾到皮肤或衣服上.浓硫酸在实验室常用作干燥剂,因为浓硫酸有吸水性.
(4)烧水的铝壶中常结有一层水垢(主要成分为CaCO3)用适量的稀盐酸可以除去它,反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑,若盐酸的用量过多,会损坏铝壶,反应的化学方程式是2Al+6HCl═2AlCl3+3H2↑.
分析 根据酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化物、碱、碳酸盐等反应)、浓硫酸有强烈的腐蚀性,据此进行分析解答.
解答 解:(1)根据酸的化学性质,酸能与活泼金属、金属氧化物、碱、碳酸盐等,故①中可填写活泼金属,②中可填写碱;
(2)稀盐酸与氧化铁反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;
(3)浓硫酸有强烈的腐蚀性,不要将浓硫酸沾到皮肤或衣服上.浓硫酸在实验室常用作干燥剂,因为浓硫酸有吸水性;
(4)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,盐酸和铝反应生成氯化铝和氢气,故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑,2Al+6HCl═2AlCl3+3H2↑.
故答案为:(1)①活泼金属;②碱;
(2)Fe2O3+6HCl═2FeCl3+3H2O;
(3)腐蚀性;吸水;
(4)CaCO3+2HCl═CaCl2+H2O+CO2↑,2Al+6HCl═2AlCl3+3H2↑.
点评 本题难度不大,掌握酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化物、碱、碳酸盐等反应)并能灵活运用是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列图象能正确反映所对应关系的是( )
| A. | 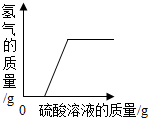 向一定量的锌粒中加入足量的稀硫酸,生成氢气和稀硫酸的质量关系 | |
| B. | 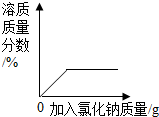 某温度下,向一定量不饱和氯化钠溶液中加入氯化钠晶体,溶质质量分数与加入氯化钠质量的关系 | |
| C. | 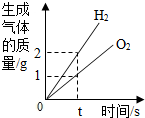 电解水时,反应时间与生成气体的质量关系 | |
| D. | 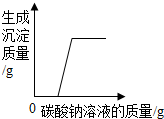 向含有一定量稀盐酸和氯化钙的混合溶液中逐滴加入碳酸钠溶液,所加碳酸钠溶液质量与生成沉淀质量的关系 |
17.氧气是我们身边常见的物质,以下关于氧气的叙述不正确的是( )
| A. | 用加热高锰酸钾的方法可以制取氧气 | |
| B. | 鱼、虾能在水中生存,证明氧气易溶于水 | |
| C. | 用带火星的木条可以检验氧气 | |
| D. | 铁丝能在氧气中燃烧,火星四溅,产生黑色固体 |
14.化学实验室需经常取用NaOH溶液,当多次揭开其瓶盖后,同学们猜想该试剂可能部分变质了,由此,大家开始了探究.
【提出问题】NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】小怡的猜想:NaOH溶液部分变质
你的新猜想:NaOH溶液全部变质.
【实验探究】小怡设计如下实验 来验证自己的猜想,请根据表中内容填写小怡实验时的现象
假设你的猜想正确,并按小怡的实验方案进行实验,则你观察到的实验现象是:只产生白色沉淀,酚酞试液不变色.
【实验反思】下列物质①Ca(NO3)2溶液、②Ca(OH)2溶液、③Ba(OH)2溶液,不能替代小怡实验中CaCl2溶液的是②③(填序号)
【提出问题】NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】小怡的猜想:NaOH溶液部分变质
你的新猜想:NaOH溶液全部变质.
【实验探究】小怡设计如下实验 来验证自己的猜想,请根据表中内容填写小怡实验时的现象
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液. | NaOH溶液部分变质 |
【实验反思】下列物质①Ca(NO3)2溶液、②Ca(OH)2溶液、③Ba(OH)2溶液,不能替代小怡实验中CaCl2溶液的是②③(填序号)
16.下列属于纯净物的是( )
| A. | 盐酸 | B. | 液氧 | C. | 玻璃钢 | D. | 生铁 |

 水是一种重要的自然资源,是生活、生产必不可少的物质.请回答下列问题:如图所示,实验Ⅰ是制备蒸馏水的装置,实验Ⅱ是电解水的装置.
水是一种重要的自然资源,是生活、生产必不可少的物质.请回答下列问题:如图所示,实验Ⅰ是制备蒸馏水的装置,实验Ⅱ是电解水的装置.