题目内容
9.20℃时,氯化钠饱和溶液中溶质.溶剂、溶液的质量比是9:25:34.(20℃时氯化钠的溶解度是36g)分析 溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量,据此进行分析解答.
解答 解:20℃时氯化钠的溶解度是36g,其涵义是20℃时,100g水中最多溶解36g氯化钠,溶液达到饱和状态,则20℃时,氯化钠饱和溶液中溶质、溶剂、溶液的质量比是36g:100g:136g=9:25:34.
故答案为:9:25:34.
点评 本题难度不大,理解溶解度的概念,熟记溶解度的四要素(温度、100g溶剂、饱和状态、单位是克)是正确解答本题的关键.

练习册系列答案
相关题目
17.有NaCl、MgCl2、FeCl3三种溶液,分别与AgNO3溶液反应,生成的AgCl沉淀的质量刚好相等,则消耗溶质AgNO3的质量比是( )
| A. | 1:2:3 | B. | 3:2:1 | C. | 2:3:6 | D. | 1:1:1 |
1.下列物质间的转化不能都通过一步反应实现的是( )
| A. | Fe→FeCl3→Cu | B. | NaOH→H2O→Ca(OH)2 | C. | O2→H2O→O2 | D. | CuSO4→Cu→CuO |
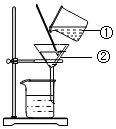 (1)写出仪器名称①烧杯②漏斗.
(1)写出仪器名称①烧杯②漏斗.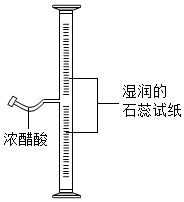 如图所示,在粗玻璃管内壁上粘附湿润的石蕊试纸,向细玻璃管里滴入数滴浓醋酸后,立即封闭管口.10s后即观察到:仅有中下部的石蕊试纸从上往下逐渐变色.
如图所示,在粗玻璃管内壁上粘附湿润的石蕊试纸,向细玻璃管里滴入数滴浓醋酸后,立即封闭管口.10s后即观察到:仅有中下部的石蕊试纸从上往下逐渐变色.