题目内容
 如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.
如图为“хх”钙片商品标签图,请根据标签的有关信息完成下列各题.(1)主要成分碳酸钙(CaCO3)由
(2)碳酸钙中各元素的质量比为
(3)每片钙片中含钙元素的质量至少为多少(要计算过程)?
考点:标签上标示的物质成分及其含量,化学式的书写及意义,元素质量比的计算,化合物中某元素的质量计算
专题:标签图示型
分析:(1)根据物质的组成来分析;
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据“每片钙片中含碳酸钙的质量×碳酸钙中钙元素的质量分数”计算即可.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据“每片钙片中含碳酸钙的质量×碳酸钙中钙元素的质量分数”计算即可.
解答:解:(1)由碳酸钙的化学式可知,它是由碳、氢、氧三种元素组成的,故填:三;
(2)碳酸钙中钙、碳、氧三种元素的质量比为40:12:(16×3)=10:3:12.故填:10:3:12;
(3)每片钙片中至少含钙元素的质量为:1.5g×
×100%=0.6g.
故填:0.6g.
(2)碳酸钙中钙、碳、氧三种元素的质量比为40:12:(16×3)=10:3:12.故填:10:3:12;
(3)每片钙片中至少含钙元素的质量为:1.5g×
| 40 |
| 100 |
故填:0.6g.
点评:本题主要考查学生运用化学式和元素的质量分数公式进行计算的能力.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
对实验的相关内容分析判断不正确的是( )
| A、蜡烛燃烧的过程既有物理变化,又有化学变化 |
| B、证明呼出气体含水蒸气多的证据是:呼出的气体在玻璃上结出水珠 |
| C、蜡烛在空气中燃烧属于化合反应 |
| D、证明呼出气体含二氧化碳多的证据是:呼出的气体使澄清石灰水变浑浊 |
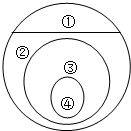 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若最大圆圈代表纯净物,下列选项正确的是( )
如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若最大圆圈代表纯净物,下列选项正确的是( )| A、①单质、③氧化物 |
| B、②化合物、④氧化物 |
| C、①单质、③化合物 |
| D、②含氧化合物、④氧化物 |
下列实验操作能达到预期目的是( )
| A、用闻气味的方法鉴别CO和CO2气体 |
| B、除去空气中的氧气又不引入新的杂质气体可用红热的木炭 |
| C、用托盘天平称取3.27g NaCl固体 |
| D、用排水法收集氧气 |
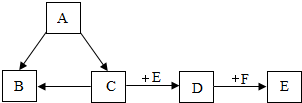 如图是A、B、C、D、E、F六种物质问的关系(“→”表示物质间的转化关系,部分反应条件和生成物省略).A、B、D是氧化物,且A、B为无色液体,C、E、F是单质,D、F为黑色固体.
如图是A、B、C、D、E、F六种物质问的关系(“→”表示物质间的转化关系,部分反应条件和生成物省略).A、B、D是氧化物,且A、B为无色液体,C、E、F是单质,D、F为黑色固体.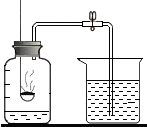 已知空气的主要成分是氮气和氧气,某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气,某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示: