题目内容
16.下列物质由分子构成的是( )| A. | 食盐 | B. | 二氧化碳 | C. | 铁 | D. | 金刚石 |
分析 根据金属、大多数固态非金属单质、稀有气体等由原子构成;有些物质是由分子构成的,气态的非金属单质和由非金属元素组成的化合物,如氢气、水等;有些物质是由离子构成的,一般是含有金属元素和非金属元素的化合物,如氯化钠,进行分析判断即可.
解答 解:A、食盐是由钠离子和氯离子构成的,故选项错误.
B、二氧化碳是由二氧化碳分子构成的,故选项正确.
C、铁属于金属单质,是由铁原子直接构成的,故选项错误.
D、金刚石属于固态非金属单质,是由碳原子直接构成的,故选项错误.
故选:B.
点评 本题难度不大,主要考查了构成物质的微观粒子方面的知识,对物质进行分类与对号入座、掌握常见物质的粒子构成是正确解答本题的关键.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案
相关题目
7.推理是化学学习中常用的方法,以下推理的相关结论正确的是( )
| A. | 碱的水溶液显碱性,所以碱性溶液一定是碱溶液 | |
| B. | 化合物是由不同种元素组成的纯净物,所以只含一种元素的物质一定不是化合物 | |
| C. | 缓慢氧化和剧烈的氧化反应均放热,所以有热量产生的变化均属于氧化反应 | |
| D. | 分子在永不停息地运动,所以水往低处流说明分子在不停地运动 |
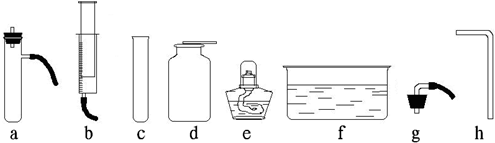
1.利用下列仪器进行实验(所有装置的气密性都已检查完毕)
(1)把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并收集氧气,完成该实验你所选用的仪器有abdh(填字母).写出发生反应的文字表达式式过氧化氢$\stackrel{二氧化锰}{→}$氧气+水.这种方法与“把二氧化锰加入盛有过氧化氢溶液的试管中制氧气”相比有产生氧气的速率均匀或可以得到平稳的氧气流等的优点.
(2)某同学继续探究“红砖粉末是否也可以作过氧化氢分解的催化剂?”实验步骤和现象如下:
①他分别向两支试管中加入等质量等溶质质量分数的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快.
②将反应较快的试管内固体过滤出来,洗涤、烘干、称量.
③用称量后的固体重复步骤①的实验,现象与步骤①完全相同.
试回答:步骤①中他除了选用试管外还用到上面列出的仪器有fgh(填字母).步骤③的实验目的是证明红砖粉末在反应前后的化学性质没有改变.该学生认为通过上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为该同学的实验还缺少一个关键步骤,请指出来实验开始没有称量红砖粉末的质量.可以用注射器代替的仪器是:胶头滴管和量筒
(3)以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
(1)通过实验①和②对比可知,化学反应快慢与过氧化氢的浓度有关;
(2)通过对比实验③和④可知,化学反应快慢与温度的关系是温度越高反应速度越快,温度越低反应速度越慢.
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是20℃时5%过氧化氢溶液中加入少量二氧化锰.
(4)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可)
(1)把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并收集氧气,完成该实验你所选用的仪器有abdh(填字母).写出发生反应的文字表达式式过氧化氢$\stackrel{二氧化锰}{→}$氧气+水.这种方法与“把二氧化锰加入盛有过氧化氢溶液的试管中制氧气”相比有产生氧气的速率均匀或可以得到平稳的氧气流等的优点.
(2)某同学继续探究“红砖粉末是否也可以作过氧化氢分解的催化剂?”实验步骤和现象如下:

①他分别向两支试管中加入等质量等溶质质量分数的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快.
②将反应较快的试管内固体过滤出来,洗涤、烘干、称量.
③用称量后的固体重复步骤①的实验,现象与步骤①完全相同.
试回答:步骤①中他除了选用试管外还用到上面列出的仪器有fgh(填字母).步骤③的实验目的是证明红砖粉末在反应前后的化学性质没有改变.该学生认为通过上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为该同学的实验还缺少一个关键步骤,请指出来实验开始没有称量红砖粉末的质量.可以用注射器代替的仪器是:胶头滴管和量筒
(3)以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/0C | 二氧化锰用量/g | 氧气体积/ml | 反应所需时间/s |
| ① | 5 | 12 | 20 | 0.2 | 125 | 11 |
| ② | 30 | 12 | 20 | 0.2 | 125 | 2 |
| ③ | 30 | 12 | 40 | / | 125 | 148 |
| ④ | 30 | 12 | 90 | / | 125 | 82 |
(2)通过对比实验③和④可知,化学反应快慢与温度的关系是温度越高反应速度越快,温度越低反应速度越慢.
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是20℃时5%过氧化氢溶液中加入少量二氧化锰.
(4)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可)
8.“人造空气”帮助人类实现了“太空漫步”的理想,其中含有70%的N2,20%以上的O2,还有CO2等,下列说法正确的是( )
| A. | “人造空气”比空气中的氧气含量高 | |
| B. | 燃着的蜡烛在“人造空气”中会熄灭 | |
| C. | “人造空气”若只含有O2会更有益于人的呼吸 | |
| D. | 加热铜丝,铜丝表面会变成黑色,可以利用反应铜+氧气$\stackrel{加热}{→}$氧化铜测定“人造空气”中O2的含量 |