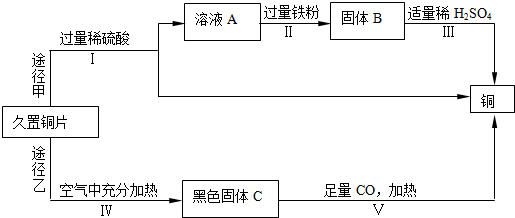
题目内容
14.生活中的下列物品加入适量水后,可以形成溶液的是( )| A. | 冰块 | B. | 蔗糖 | C. | 面粉 | D. | 奶油 |
分析 本题考查溶液的概念,在一定条件下溶质分散到溶剂中形成的是均一稳定的混合物.
解答 解:A、冰块放入水中属于纯净物,不属于溶液,故A错;
B、蔗糖易溶于水,形成均一、稳定的混合物,属于溶液,故B正确;
C、面粉不溶于水,形成悬浊液,不能形成溶液,故C错;
D、奶油不溶于水,形成的是浊液,故D错.
故选B.
点评 应熟悉溶液是一种均一稳定的混合物,在不改变条件时,溶液的组成和浓度都不会发生变化,要与悬浊液和乳浊液区分.

练习册系列答案
相关题目
2.下列对有关事实的解释中,错误的是( )
| A. | 生铁和钢的性能不同--含碳量不同 | |
| B. | CO和C02的化学性质不同--分子构成不同 | |
| C. | 钠原子和钠离子化学性质不同--质子数不同 | |
| D. | 金刚石和石墨的物理性质不同--原子排列方式不同 |
9.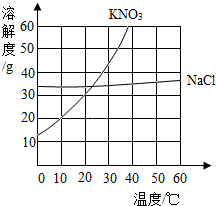 根据给出的KNO3和NaCl两种物质的溶解度表及溶解度曲线,回答问题.
根据给出的KNO3和NaCl两种物质的溶解度表及溶解度曲线,回答问题.
(1)在60℃时,KNO3的溶解度为110g;
(2)由以上信息可知,从海水中提取氯化钠,通常采用的方法是蒸发结晶;
(3)从溶解度表中可知,NaC1和KNO3溶解度相差较小的温度是20℃.
(4)80℃时,100克水中溶解KNO3达到饱和状态,降温至60℃有59gKNO3析出.
 根据给出的KNO3和NaCl两种物质的溶解度表及溶解度曲线,回答问题.
根据给出的KNO3和NaCl两种物质的溶解度表及溶解度曲线,回答问题.| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)由以上信息可知,从海水中提取氯化钠,通常采用的方法是蒸发结晶;
(3)从溶解度表中可知,NaC1和KNO3溶解度相差较小的温度是20℃.
(4)80℃时,100克水中溶解KNO3达到饱和状态,降温至60℃有59gKNO3析出.
19. 铟具有光渗透性和强导电性,广泛用于生产液晶显示器.元素周期表中“铟”的信息如图所示.下列关于铟元素说法,错误的是( )
铟具有光渗透性和强导电性,广泛用于生产液晶显示器.元素周期表中“铟”的信息如图所示.下列关于铟元素说法,错误的是( )
 铟具有光渗透性和强导电性,广泛用于生产液晶显示器.元素周期表中“铟”的信息如图所示.下列关于铟元素说法,错误的是( )
铟具有光渗透性和强导电性,广泛用于生产液晶显示器.元素周期表中“铟”的信息如图所示.下列关于铟元素说法,错误的是( )| A. | 是非金属元素 | B. | 元素符号为Ir | ||
| C. | 相对原子质量为114.82 | D. | 原子序数为49 |
6.石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如表:
(1)该石灰石样品中碳酸钙的质量分数是75%;
(2)计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%).
(3)第三次加入5g稀盐酸后所得溶液的质量为16.68g.
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 稀盐酸的用量 | 5g | 5g | 5g | 5g |
| 剩余固体的质量 | 3g | 2g | 1g | 1g |
(2)计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%).
(3)第三次加入5g稀盐酸后所得溶液的质量为16.68g.
3.钠是一种活泼的金属,将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)$\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$氢氧化钠溶液$\stackrel{CO_{2}}{→}$白色固体
[提出问题]:常温下钠与氧气反应,产物有哪些?
[查阅资料]:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
[作出猜想]:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:Na2O和Na2O2
[实验探究一]:
[继续探究]:钠在空气中放置一段时间得到白色固体的成分
[作出猜想]
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
[实验探究二]:
[反思与拓展]
(1)类比Na2O+H2O═2NaOH;Na2O+CO2═Na2CO3;类比2Na2O2+2H2O═4NaOH+O2↑,写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2═2Na2CO3+O2,消防服的呼吸面具中“氧气再生剂”的主要成分是淡黄色固体过氧化钠,则氧气再生剂的保存方法是密封存在干燥处.
(2)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
钠(Na)$\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$氢氧化钠溶液$\stackrel{CO_{2}}{→}$白色固体
[提出问题]:常温下钠与氧气反应,产物有哪些?
[查阅资料]:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
[作出猜想]:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:Na2O和Na2O2
[实验探究一]:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 无气泡生成 | 猜想1正确 |
[作出猜想]
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
[实验探究二]:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量白色固体加入足量CaCl2 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 过滤、取少量滤液加入无色酚酞试液 | 试液变红 |
(1)类比Na2O+H2O═2NaOH;Na2O+CO2═Na2CO3;类比2Na2O2+2H2O═4NaOH+O2↑,写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2═2Na2CO3+O2,消防服的呼吸面具中“氧气再生剂”的主要成分是淡黄色固体过氧化钠,则氧气再生剂的保存方法是密封存在干燥处.
(2)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2不是碱性氧化物(填“是”或“不是”).
4.化学与生活、社会密切相关.下列说法不正确的是( )
| A. | 施用熟石灰改良酸性土壤时,不宜同时施用碳酸氢铵 | |
| B. | 不吃水果蔬菜,多吃含蛋白质的肉类,更能增强体质 | |
| C. | 为防止电池中的重金属等污染土壤和水体,积极开发废电池综合利用技术 | |
| D. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |