题目内容
16.硫酸、盐酸是重要的化工原料.(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有吸水性.
(2)写出稀硫酸转化为盐酸的化学方程式H2SO4+BaCl2═BaSO4↓+2HCl;
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是②③(填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH.
分析 (1)根据浓硫酸具有吸水性,进行分析解答.
(2)根据把硫酸转变成盐酸,即把硫酸中的硫酸根离子转变成氯离子,也就是把硫酸根离子转化成沉淀解答.
(3)盐酸、硫酸都能与金属氧化物反应;通常制作氯化锌用盐酸;除杂不得引入新的杂质.
解答 解:(1)浓硫酸具有吸水性,在实验室常用作干燥剂.
故答案是:吸水;
(2)把硫酸转变成盐酸,即把硫酸中的硫酸根离子转变成氯离子,也就是把硫酸根离子转化成沉淀,因此应加入适量的氯化钡溶液,方程式为:H2SO4+BaCl2═BaSO4↓+2HCl.
故答案是:H2SO4+BaCl2═BaSO4↓+2HCl.
(3)盐酸、硫酸都能与金属氧化物反应,都能用于金属表面除锈;不用硫酸作为制取药物氯化锌,用盐酸制造药物氯化锌;除杂不得引入新的杂质,而硫酸与氢氧化钠反应会生成新的杂质硫酸钠.
故答案是:②③
点评 本题较全面的考查了酸的性质,掌握常用的盐酸、硫酸的化学性质及反应原理是解答此类题的关键,同时注意除杂时,在除掉杂质的基础上不得引入新的杂质.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
6.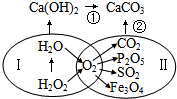 如图是表示了初中化学常见物质间相互转化关系(反应条件己省略).下列说法错误的是( )
如图是表示了初中化学常见物质间相互转化关系(反应条件己省略).下列说法错误的是( )
 如图是表示了初中化学常见物质间相互转化关系(反应条件己省略).下列说法错误的是( )
如图是表示了初中化学常见物质间相互转化关系(反应条件己省略).下列说法错误的是( )| A. | 圈I中发生的反应可能都是分解反应 | |
| B. | 利用反应②可用来检验二氧化碳气体 | |
| C. | 圈Ⅱ中的化学反应说明氧气具有可燃性 | |
| D. | 利用反应①可制得烧碱 |
7.下列实验操作错误的是( )
| A. | 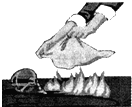 酒精灯失火用湿布铺盖 | B. | 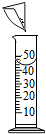 将NaCl倒入量筒中配制溶液 | ||
| C. |  加碱研磨后闻气味鉴别铵态氮肥 | D. | 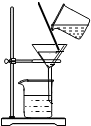 分离溶液中析出的KNO3 |
4.某研究学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品20g,把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应).根据实验数据计算:(计算结果保留到小数点后一位.)
(1)表中n的数值为6.8.
(2)样品中碳酸钙的质量分数是多少?
(3)求盐酸中溶质的质量分数是多少?
| 实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 1 | 20 | 15 |
| 2 | 20 | 10 |
| 3 | 20 | 6.8 |
| 4 | 20 | n |
(2)样品中碳酸钙的质量分数是多少?
(3)求盐酸中溶质的质量分数是多少?
1.下列化学符号中数字“2”表示的意义正确的是( )
| A. | 2Fe3+:两个亚铁离子 | B. | $\stackrel{+2}{Cu}$:一个铜离子带2个单位正电荷 | ||
| C. | 2H:两个氢元素 | D. | O2:一个氧分子中含有两个氧原子 |
1.下列应用,对应的化学方程式、所属基本反应类型都正确的是( )
| A. | 用X射线检查胃肠时,让病人服用钡餐:BaCO3+2HCl═BaCl2+H2O+CO2↑复分解反应 | |
| B. | 美丽的溶洞中钟乳石的形成:Ca(HCO3)2═CaCO3↓+CO2↑+H2O 分解反应 | |
| C. | 用木炭测空气中氧气含量:C+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2 化合反应 | |
| D. | 用铁桶盛装稀硫酸:Fe+H2SO4═FeSO4+H2↑ 置换反应 |