题目内容
15.2004年4月15日,重庆天元化工厂发生氯气(Cl2)泄漏事故,继而发生氯气罐爆炸,周围十五万群众紧急撤离.氯气是一种黄绿色、有毒、有剧烈刺激性气味的气体,相同情况下密度比空气大,能溶于水,并与水反应生成盐酸(HCl)和次氯酸(HClO).(1)根据以上信息,氯气的物理性质有黄绿色、有剧烈刺激性气味的气体(或密度比空气大,能溶于水).(至少2点)
(2)消防队员用高压水枪溶解弥漫空气中的氯气,写出氯气与水反应的化学方程式:Cl2+H2O=HCl+HClO
(3)将氯气通入含氢氧化钙Ca(OH)2的水池中,使氯气不再对周围居民造成伤害.已知氯气与Ca(OH)2的反应方程式为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2X,则X的化学式H2O.
分析 (1)根据物理性质的定义进行分析;
(2)根据化学方程式的书写方法考虑;
(3)依据质量守恒定律中化学反应前后原子的种类及个数不会改变判断X的化学式;
解答 解:(1)由物理性质的定义及题中给出的信息可知,氯气的黄绿色,有剧烈刺激性气味的气体,密度比空气大,能溶于水的性质,不需要发生化学变化就表现出来的性质,属于物理性质;
(2)反应物是氯气和水,生成物是盐酸和次氯酸,所以方程式是:Cl2+H2O=HCl+HClO;
(3)依据质量守恒定律中化学反应前后原子的种类及个数不会改变可知:反应前氯、钙、氧和氢的原子个数分别是4、2、4和4,而反应后氯、钙和氧的原子个数分别是4、2和2,所以X的化学式应为H2O;
故答为:(1)黄绿色;有剧烈刺激性气味的气体(或密度比空气大,能溶于水);(2)Cl2+H2O=HCl+HClO;(3)H2O.
点评 本题属于新信息试题,考查同学们信息读取、处理能力和灵活运用所学知识解决问题的能力.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
6.钢铁工业是国家工业的基础.
(1)如图1是教材中炼铁高炉及炉内化学变化过程示意图,根据图示回答下列问题.
若图中采用的铁矿石的主要成分为氧化铁,请写出炼铁反应的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)出铁口流出的铁水分类上属于混合物.(纯净物、混合物)
【设计实验】
实验室制备纯净的一氧化碳,用一氧化碳还原氧化铁粉末的实验如下图2、图3,图2中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:H2C2O4$\frac{\underline{\;H_{2}SO_{4}\;}}{△}$CO↑+CO2↑+H2O.
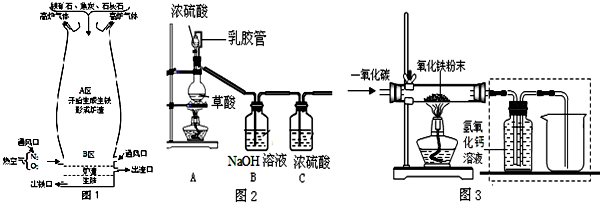
请回答下列问题:
(1)图2中,A 装置中乳胶管的作用是使上下压强相等,便于浓硫酸流下.
(2)按图3实验时,应该先通CO.(填“通CO”或“点燃酒精灯”)
【进行实验】
该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
【分析与讨论】
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
【查阅资料】
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
【实验与猜想】①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能是以下三种情况:
甲:全部为铁; 乙:全部为四氧化三铁;丙:铁和四氧化三铁的混合物.
【得出结论】通过实验中获得的数据进行计算:
(1)生成的黑色固体粉末的质量为5.8g.
(2)由计算判断乙猜想是正确的(填甲、乙、丙).
【反思与评价】①一氧化碳还原氧化铁实验中,若要得到铁可适当提高反应温度和延长反应时间.同时结束时应先熄灭酒精喷灯,再停止通入CO,防止铁被继续氧化.
②实验装置图中采用虚线框内的装置,其作用有AC
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
(1)如图1是教材中炼铁高炉及炉内化学变化过程示意图,根据图示回答下列问题.
若图中采用的铁矿石的主要成分为氧化铁,请写出炼铁反应的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)出铁口流出的铁水分类上属于混合物.(纯净物、混合物)
【设计实验】
实验室制备纯净的一氧化碳,用一氧化碳还原氧化铁粉末的实验如下图2、图3,图2中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:H2C2O4$\frac{\underline{\;H_{2}SO_{4}\;}}{△}$CO↑+CO2↑+H2O.

请回答下列问题:
(1)图2中,A 装置中乳胶管的作用是使上下压强相等,便于浓硫酸流下.
(2)按图3实验时,应该先通CO.(填“通CO”或“点燃酒精灯”)
【进行实验】
该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
【分析与讨论】
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
【查阅资料】
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
| 物质, 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
②进行猜想:黑色固体粉末可能是以下三种情况:
甲:全部为铁; 乙:全部为四氧化三铁;丙:铁和四氧化三铁的混合物.
【得出结论】通过实验中获得的数据进行计算:
(1)生成的黑色固体粉末的质量为5.8g.
(2)由计算判断乙猜想是正确的(填甲、乙、丙).
【反思与评价】①一氧化碳还原氧化铁实验中,若要得到铁可适当提高反应温度和延长反应时间.同时结束时应先熄灭酒精喷灯,再停止通入CO,防止铁被继续氧化.
②实验装置图中采用虚线框内的装置,其作用有AC
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
3.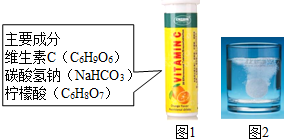 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2),该小组同学进行如下研究.
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2),该小组同学进行如下研究.
探究一:该气体的成分.
【猜想与假设】
小华说:该气体可能是CO2、O2、CO、H2、N2.
小明说:不可能含有N2,因为根据化学反应前后元素种类不变,反应物中不含氮元素.
小芳说:不可能含有H2,因为从药品安全角度考虑,H2易燃易爆,同时也不能含有CO.
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
【得出结论】
(1)由实验①可知,该气体中肯定含有二氧化碳.
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.
探究二:维C泡腾片溶液的酸碱性.向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性.
 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2),该小组同学进行如下研究.
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2),该小组同学进行如下研究.探究一:该气体的成分.
【猜想与假设】
小华说:该气体可能是CO2、O2、CO、H2、N2.
小明说:不可能含有N2,因为根据化学反应前后元素种类不变,反应物中不含氮元素.
小芳说:不可能含有H2,因为从药品安全角度考虑,H2易燃易爆,同时也不能含有CO.
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(1)由实验①可知,该气体中肯定含有二氧化碳.
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.
探究二:维C泡腾片溶液的酸碱性.向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性.
4.高层建筑着火时,高压水枪起着重要灭火作用,水能灭火的主要原因是( )
| A. | 降低可燃物的温度 | B. | 降低可燃物的着火点 | ||
| C. | 使可燃物隔绝氧气 | D. | 使可燃物与货源隔离 |
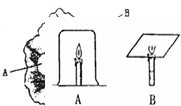 小明在学校科学实验室对蜡烛的蜡的组成成分进行实验探究:
小明在学校科学实验室对蜡烛的蜡的组成成分进行实验探究: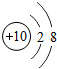
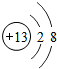


 碘元素是人体必需的微量元素之一.如图是元素周期表中碘元素的部分信息.碘原子的核电荷数是53碘元素属于非金属(填“金属”或“非金属”)元素.
碘元素是人体必需的微量元素之一.如图是元素周期表中碘元素的部分信息.碘原子的核电荷数是53碘元素属于非金属(填“金属”或“非金属”)元素.