题目内容
14.化学上研究任何一种物质的性质,都必须取用纯净物.下列属于纯净物的是 ( )| A. | 空气 | B. | 过氧化氢溶液 | C. | 二氧化碳 | D. | 矿泉水 |
分析 本题考查利用纯净物的概念来判断物质是否为纯净物,宏观上看只有一种物质,微观上只有一种分子.
解答 解:A、空气中含有氧气、氮气、二氧化碳等物质,属于混合物,故A错;
B、过氧化氢溶液中含有过氧化氢和水,属于混合物,故B错;
C、二氧化碳是由一种物质组成,属于纯净物,故C正确;
D、矿泉水中含有水和多种矿物质,属于混合物,故D错.
故选C.
点评 在熟悉概念的基础上能从宏观和微观两个方面来判断纯净物和混合物,还要从社会实践中了解生活中常见物质的组成.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
4.实验室用98%的浓硫酸配制成稀硫酸,并与锌粒反应制取氢气.
(1)查阅资料:20℃时不同质量分数硫酸的密度(g/mL)如下表
分析以上数据,可以得出结论(任写1条)硫酸溶液中溶质的质量分数越大,溶液的密度越大(或硫酸溶液的密度比纯水的密度大);.
(2)计算:配制200g24.5%的稀硫酸,需98%浓硫酸多少毫升?请列式:V==$\frac{200g×24.5%}{98%×1.84g/mL}$(只列式不要求计算)
(3)配制稀硫酸:分别用量筒量取所需水和浓硫酸,先将水倒入烧杯中,再将浓硫酸沿着烧杯壁缓缓倒入,并用玻璃棒不断搅拌.
(1)查阅资料:20℃时不同质量分数硫酸的密度(g/mL)如下表
| 质量分数 | 4% | 10% | 16% | 24% | 32% | 36% | 44% | 49% | 60% | 98% |
| 密度 | 1.02 | 1.07 | 1.11 | 1.17 | 1.24 | 1.27 | 1.34 | 1.39 | 1.50 | 1.84 |
(2)计算:配制200g24.5%的稀硫酸,需98%浓硫酸多少毫升?请列式:V==$\frac{200g×24.5%}{98%×1.84g/mL}$(只列式不要求计算)
(3)配制稀硫酸:分别用量筒量取所需水和浓硫酸,先将水倒入烧杯中,再将浓硫酸沿着烧杯壁缓缓倒入,并用玻璃棒不断搅拌.
9.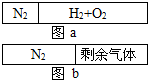 在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室.左室充入氮气,右室充入氢气与氧气的混和气体,活塞恰好停留在离左端的四分之一处(图a),然后引燃氢、氧混和气体,反应完毕后恢复至原来温度,活塞恰好停在中间(图b),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是( )
在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室.左室充入氮气,右室充入氢气与氧气的混和气体,活塞恰好停留在离左端的四分之一处(图a),然后引燃氢、氧混和气体,反应完毕后恢复至原来温度,活塞恰好停在中间(图b),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是( )
 在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室.左室充入氮气,右室充入氢气与氧气的混和气体,活塞恰好停留在离左端的四分之一处(图a),然后引燃氢、氧混和气体,反应完毕后恢复至原来温度,活塞恰好停在中间(图b),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是( )
在20℃时,在一刚性容器内部有一个不漏气且可滑动的活塞将容器分隔成左右两室.左室充入氮气,右室充入氢气与氧气的混和气体,活塞恰好停留在离左端的四分之一处(图a),然后引燃氢、氧混和气体,反应完毕后恢复至原来温度,活塞恰好停在中间(图b),如果忽略水蒸气体积,则反应前氢气与氧气的体积比可能是( )| A. | 3:4 | B. | 1:1 | C. | 2:1 | D. | 7:2 |
6.下列对如图所示实验的分析正确的是( )
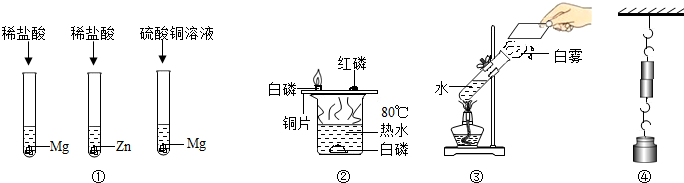

| A. | ①通过实验可以判断三种金属的活动性顺序为Mg、Zn、Cu | |
| B. | ②通过铜片上白磷、红磷的现象,说明燃烧需要氧气 | |
| C. | ③试管口出现白雾,管内的气体对塞子做功内能减少 | |
| D. | ④端面磨平的铅块压紧后能吊住大钩码,说明分子在不停地做无规则运动 |
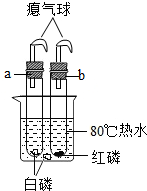 如图是学习活动小组探究可燃物燃烧需要满足的条件的实验装置.(查阅资料,可知白鳞着火点为40℃,红磷的着火点为240℃)将a、b试管放入80℃热水中,请你参与并会回答下列问题:
如图是学习活动小组探究可燃物燃烧需要满足的条件的实验装置.(查阅资料,可知白鳞着火点为40℃,红磷的着火点为240℃)将a、b试管放入80℃热水中,请你参与并会回答下列问题: