题目内容
某同学将12g大理石放入盛有50g稀盐酸的烧杯中,结果恰好完全反应.经测定反应后烧杯中溶液质量为55.6g.请计算:该大理石中碳酸钙的质量分数.
【答案】分析:运用差量法分析,反应后溶液质量与反应前溶液质量之差与碳酸钙质量成正比.根据反应前后溶液质量的变化量求出碳酸钙质量,进而求出大理石中碳酸钙的质量分数
解答:解:设大理石中碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑△溶液质量变化
100 44 100-44=56
x 55.6g-50g

x=10g
大理石中碳酸钙的质量分数为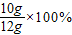 =83.3%
=83.3%
答:大理石中碳酸钙的质量分数为83.3%
点评:本题考查根据化学方程式的计算以及守恒法的运用,本题难点分析反应前后溶液质量的变化量与碳酸钙之间的关系,根据题中溶液质量列出方程
解答:解:设大理石中碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑△溶液质量变化
100 44 100-44=56
x 55.6g-50g

x=10g
大理石中碳酸钙的质量分数为
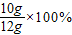 =83.3%
=83.3%答:大理石中碳酸钙的质量分数为83.3%
点评:本题考查根据化学方程式的计算以及守恒法的运用,本题难点分析反应前后溶液质量的变化量与碳酸钙之间的关系,根据题中溶液质量列出方程

练习册系列答案
相关题目