题目内容
3.如图中所示物质的pH,判断下列说法正确的是( )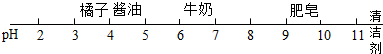
| A. | 清洁剂显碱性 | B. | 肥皂液再加水稀释后pH变大 | ||
| C. | 牛奶酸性比酱油强 | D. | 胃酸过多的人可多吃橘子 |
分析 当溶液的pH等于7时,呈中性.当溶液的pH大于7时,呈碱性.当溶液的pH小于7时,呈酸性.
解答 解:A、清洁剂的pH大于7,显碱性.正确;
B、肥皂液的pH大于7,显碱性,肥皂液再加水稀释后pH变小,碱性变弱.错误;
C、牛奶的pH大于酱油的pH,酸性比酱油弱.错误;
D、橘子的pH小于7,显酸性,胃酸过多的人不宜多吃橘子.错误.
故选A.
点评 本题考查了溶液的酸碱性于pH的关系,解答此题,需要依据已有的知识进行.

练习册系列答案
相关题目
4.下列变化属于化学变化的是( )
| A. | 干冰升华 | B. | 石蜡熔化 | C. | 光合作用 | D. | 海水晒盐 |
11.造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )
| A. | 分子很小 | B. | 分子由原子构成 | C. | 分子之间有间隙 | D. | 分子在不断运动 |
18.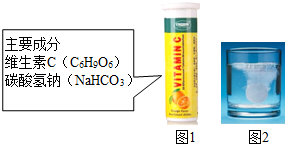 维C泡腾片是一种保健药品(主要成分见图1),溶于水有许多气泡产生(如图2)某兴趣小组对该气体的成分进行如下探究.
维C泡腾片是一种保健药品(主要成分见图1),溶于水有许多气泡产生(如图2)某兴趣小组对该气体的成分进行如下探究.
【假设】有的同学提出该气体可能是H2、O2、N2、CO、CO2
【讨论】经过分析讨论,大家初步取得如下共识:
(1)根据质量守恒定律,该气体不可能含有N2.
(2)从药品安全角度考虑,不可能含有CO和H2,因为H2易燃易爆,CO有毒.
(3)该气体可能含有CO2、O2中的一种或两种.
【实验】
【结论】(1)由实验①可知.该气体中肯定含有二氧化碳.写出该反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.若要证明是否含有氧气,你的实验方案是将气体先通过氢氧化钠溶液然后将带火星的木条伸入该气体中 观察是否复燃.
 维C泡腾片是一种保健药品(主要成分见图1),溶于水有许多气泡产生(如图2)某兴趣小组对该气体的成分进行如下探究.
维C泡腾片是一种保健药品(主要成分见图1),溶于水有许多气泡产生(如图2)某兴趣小组对该气体的成分进行如下探究.【假设】有的同学提出该气体可能是H2、O2、N2、CO、CO2
【讨论】经过分析讨论,大家初步取得如下共识:
(1)根据质量守恒定律,该气体不可能含有N2.
(2)从药品安全角度考虑,不可能含有CO和H2,因为H2易燃易爆,CO有毒.
(3)该气体可能含有CO2、O2中的一种或两种.
【实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑法 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(2)由实验②不能(填“能”或“不能”)确定该气体中不含氧气,理由是若生成氧气和二氧化碳的混合物,当氧气含量过少时,带火星的木条也不能复燃.若要证明是否含有氧气,你的实验方案是将气体先通过氢氧化钠溶液然后将带火星的木条伸入该气体中 观察是否复燃.
8.下列图象能正确反映其对应实验操作的是( )
| A. |  在恒温的条件下,将氯化钠不饱和溶液蒸发适量的水分 在恒温的条件下,将氯化钠不饱和溶液蒸发适量的水分 | |
| B. | 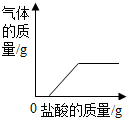 向生锈程度较大的铁钉中加入过量稀盐酸 向生锈程度较大的铁钉中加入过量稀盐酸 | |
| C. |  向氢氧化钠溶液中不断滴加稀盐酸 向氢氧化钠溶液中不断滴加稀盐酸 | |
| D. | 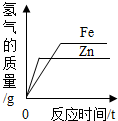 相同质量的且过量的锌粉和铁粉,分别于质量和质量分数相同的稀盐酸反应 相同质量的且过量的锌粉和铁粉,分别于质量和质量分数相同的稀盐酸反应 |
15.某同学为了测定NaCl和MgCl2固体混合物中MgCl2的质量分数,进行如下实验:将80g固体混合物溶于水配成溶液,平均分成四份,分别加入相同质量分数的NaOH溶液,获得如下实验数据:
问:
(1)表中m的值为5.8;
(2)原固体混合物中MgCl2的质量分数是多少?
(3)加入氢氧化钠溶液的溶质质量分数是多少?
| 实验次数 | 一 | 二 | 三 | 四 |
| 固体混合物的质量(g) | 20 | 20 | 20 | 20 |
| 加入NaOH溶液的质量(g) | 20 | 40 | 60 | 80 |
| 生成沉淀的质量(g) | 2.9 | m | 8.7 | 8.7 |
(1)表中m的值为5.8;
(2)原固体混合物中MgCl2的质量分数是多少?
(3)加入氢氧化钠溶液的溶质质量分数是多少?
13.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动,以下是教学片断,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】(1)该反应的化学方程式H2SO4+2NaOH═Na2SO4 +2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】(2)针对疑问,大家纷纷提出猜想.
甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四.
【实验探究】(3)①丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH或氢氧化钠.
②为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出【实验探究】(4)②中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:①实验操作中的错误是pH试纸浸入溶液中.②实验方案中也有一个是错误的,错误的原因是BaCl2与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】(1)该反应的化学方程式H2SO4+2NaOH═Na2SO4 +2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】(2)针对疑问,大家纷纷提出猜想.
甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四.
【实验探究】(3)①丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH或氢氧化钠.
②为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  | 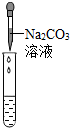 | 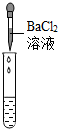 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生; | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出【实验探究】(4)②中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:①实验操作中的错误是pH试纸浸入溶液中.②实验方案中也有一个是错误的,错误的原因是BaCl2与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
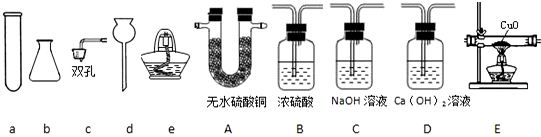
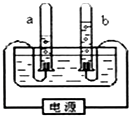 请结合如图思考并回答下列问题:
请结合如图思考并回答下列问题: