题目内容
11.写出配平下列化学方程式①2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O
②4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3.
分析 根据已有的化学反应的书写方法以及配平方法进行分析解答即可
解答 解:①该反应采用定一法,则让前面的系数为1,则二氧化碳前面的数字为2,水前面的数字为1,氧气前面的数字为$\frac{5}{2}$,同时乘以2,则该反应的化学方程式为:2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$ 4CO2+2H2O,故填:2,5,4,2;
②采用最小公倍数法,以氧原子为配平的起点,最小公倍数为6,则氧气前面的数字为3,氧化铝前面的数字为2,故铝前面的数字为4,则该反应的化学方程式为:4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$ 2Al2O3.故填:4,3,2.
点评 本题考查的是化学方程式的配平,完成此题,可以依据已有化学反应结合配平的方法进行.

练习册系列答案
相关题目
1.化学反应有不同的分类方法,关于下列反应说法正确的是( )
①2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
②8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe
③CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
④CO+CuO $\frac{\underline{\;加热\;}}{\;}$CO2+Cu.
①2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
②8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe
③CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
④CO+CuO $\frac{\underline{\;加热\;}}{\;}$CO2+Cu.
| A. | ①属于化合反应 | B. | ②属于置换反应 | C. | ③属于复分解反应 | D. | ④属于置换反应 |
19.世界上每年因锈蚀而报废的金属设备和材料,高达产量的20%~40%,某实验小组对铁的燃烧和锈蚀进行如下探究.
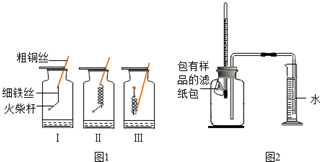
探究一:铁丝燃烧
如图1所示,取3根粗细、长度均相同的光亮细铁丝,将其中两根分别盘成螺旋状,在每根铁丝一端系上粗铜丝,另一端系一根火柴杆,点燃火柴杆待快燃尽时,分别插入充满氧气的集气瓶中,观察到:观察到:Ⅰ、Ⅱ中铁丝都剧烈燃烧,且Ⅱ中铁丝燃烧比I中的更剧烈;Ⅲ中铁丝没有燃烧.
(1)集气瓶中加入少量水的作用:防止铁燃烧时形成的高温熔融物溅落炸裂集气瓶.
(2)为什么Ⅲ中铁丝不能燃烧温度没有达到铁的着火点.
(3)分析Ⅱ中铁丝燃烧比Ⅰ中更剧烈的原因Ⅱ中铁丝与氧气的接触面积比Ⅰ中铁丝与氧气的接触面积大.
探究二:铁粉腐蚀的条件
如图2所示,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进广口瓶(容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如下表.
(4)金属腐蚀的过程实际上就是金属元素化合价升高(填“升高”或“降低”)的过程.
(5)实验①和②说明NaCl可以加快 (填“加快”或“减慢”)铁锈蚀的速率.
(6)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是放热(填“放热”或“吸热”)过程.
(7)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成是1g铁粉和10滴水.
(8)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是19.2%%(精确到小数点后1位),试分析该实验结果出现误差的原因样品不足(写任意一条即可)

探究一:铁丝燃烧
如图1所示,取3根粗细、长度均相同的光亮细铁丝,将其中两根分别盘成螺旋状,在每根铁丝一端系上粗铜丝,另一端系一根火柴杆,点燃火柴杆待快燃尽时,分别插入充满氧气的集气瓶中,观察到:观察到:Ⅰ、Ⅱ中铁丝都剧烈燃烧,且Ⅱ中铁丝燃烧比I中的更剧烈;Ⅲ中铁丝没有燃烧.
(1)集气瓶中加入少量水的作用:防止铁燃烧时形成的高温熔融物溅落炸裂集气瓶.
(2)为什么Ⅲ中铁丝不能燃烧温度没有达到铁的着火点.
(3)分析Ⅱ中铁丝燃烧比Ⅰ中更剧烈的原因Ⅱ中铁丝与氧气的接触面积比Ⅰ中铁丝与氧气的接触面积大.
探究二:铁粉腐蚀的条件
如图2所示,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进广口瓶(容积为146mL).当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零).记录起始和最终量筒的读数以及所需时间如下表.
| 序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
| 1 | 1g铁粉、0.2g碳和10滴水 | 100 | 72 | 约120 |
| 2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 72 | 约70 |
| 3 | 1g铁粉和10滴水 | \ | \ | \ |
(5)实验①和②说明NaCl可以加快 (填“加快”或“减慢”)铁锈蚀的速率.
(6)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是放热(填“放热”或“吸热”)过程.
(7)实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成是1g铁粉和10滴水.
(8)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是19.2%%(精确到小数点后1位),试分析该实验结果出现误差的原因样品不足(写任意一条即可)
16.实验室用KClO3制氧气并回收MnO2和KCl,下列操作不规范的是( )
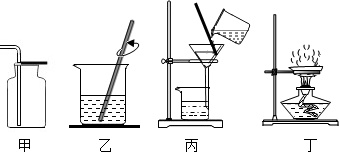

| A. | 用装置甲收集氧气 | |
| B. | 用装置乙溶解完全反应后的固体 | |
| C. | 用装置丙分离MnO2和KCl溶液 | |
| D. | 用装置丁蒸发分离后的溶液得KCl晶体 |
3.某物质中只含有一种元素,则该物质不可能是( )
| A. | 化合物 | B. | 混合物 | C. | 单质 | D. | 纯净物 |
20.下列图示的实验操作不正确的是( )
| A. |  点燃酒精灯 | B. |  检查装置的气密性 | ||
| C. |  倾倒液体 | D. |  加热液体 |

