题目内容
1.下表是几种常用燃料(1mol)完全燃烧时放出的热量:| 物质 | 炭粉(C) | 一氧化碳 (CO) | 氢气 (H2) | 甲烷 (CH4) | 乙醇 (C2H5OH) |
| 状态 | 固体 | 气体 | 气体 | 气体 | 液体 |
| 热量(kJ) | 392.8 | 282.6 | 285.8 | 890.3 | 1367 |
(2)1mol炭粉充分燃烧,需消耗氧气的物质的量是1mol;
(3)充分燃烧1mol表中各种燃料,排放出二氧化碳的量最多的是乙醇.
分析 (1)根据燃料的热值来分析;
(2)根据化学方程式来分析;
(3)根据化学方程式来分析.
解答 解:(1)从热量角度分析可知,燃烧lmol甲烷放出的热量最多,所以目前最适合家庭使用的优质气体燃料是甲烷;故答案为:甲烷;
(2)碳燃烧的化学方程式为C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,由此可见1mol炭粉充分燃烧,需消耗1mol氧气;故填:1;
(3)根据化学方程式分析如下:
C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,由此可见1mol炭粉充分燃烧,生成1mol二氧化碳;
2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2,由此可见1molCO充分燃烧,生成1mol二氧化碳;
2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,氢气燃烧不生成二氧化碳;
CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O,由此可见1mol甲烷充分燃烧,生成1mol二氧化碳;
C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,由此可见1mol酒精充分燃烧,生成2mol二氧化碳.
故答案为:乙醇.
点评 化学能源是当今社会面临的主要问题,所以在中考试题中有关此类试题较多,但是难度不大.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
12.化学实验既要操作规范,更要保障安全.下列实验基本操作符合这一要求的是( )
| A. | 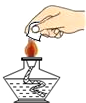 熄灭酒精灯 | B. | 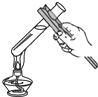 给液体加热 | C. |  闻气体气味 | D. | 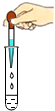 滴加液体 |
16.下列做法中,正确的是( )
| A. | 用铅笔芯作润滑剂打开生锈的铁锁 | B. | 用过滤的方法使硬水软化 | ||
| C. | 煤气泄漏时立即打开电排烟罩换气 | D. | 锅里的油着火时用水浇灭 |
1.某校化学兴趣小组的同学在探究酸碱中和反应时,将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中,反应的化学方程式是:H2SO4+2NaOH═Na2SO4 +2H2O.未观察到明显现象,部分同学对实验产生了疑问:反应后溶液中溶质是什么呢?
【提出猜想】针对疑问,小明同学作出如下猜想:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
小华同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想四.
【实验探究】同学们对剩余的猜想进行了探究:
(1)取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,学习小组的同学设计了三套实验方案:
【实验结论】经过实验探究,大家一致认为猜想二是正确的.
【实验反思】写出方案一的化学方程式:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
三个方案中有一个方案是错误的,原因是BaCl2与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【提出猜想】针对疑问,小明同学作出如下猜想:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
小华同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想四.
【实验探究】同学们对剩余的猜想进行了探究:
(1)取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,学习小组的同学设计了三套实验方案:
| 实验方案 | 取少量烧杯中溶液 | 实验现象 | 实验结论 |
| 方案一 | 加入Na2CO3溶液 | 有气泡产生 | 溶液中有H2SO4 |
| 方案二 | 滴加紫色石蕊溶液 | 溶液变红 | 溶液中有H2SO4 |
| 方案三 | 加入BaC12溶液 | 有白色沉淀生成 | 溶液中有H2SO4 |
【实验反思】写出方案一的化学方程式:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
三个方案中有一个方案是错误的,原因是BaCl2与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
5.呼吸面具中“氧气再生剂”的主要成分是淡黄色固体过氧化钠(Na2O2),使用后变成白色固体.某兴趣小组对白色固体的成分进行探究:
【查阅资料】
2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2H2O═2NaOH+O2↑
【提出猜想】根据呼出的气体中含有较多的二氧化碳和水蒸气.对白色固体作出如下猜想:猜想Ⅰ:氢氧化钠 猜想Ⅱ:碳酸钠 猜想Ⅲ:氢氧化钠和碳酸钠
【实验验证】
【得出结论】猜想Ⅲ成立
【拓展应用】“氧气再生剂”的保存方法是密封存放干燥处.
【查阅资料】
2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2H2O═2NaOH+O2↑
【提出猜想】根据呼出的气体中含有较多的二氧化碳和水蒸气.对白色固体作出如下猜想:猜想Ⅰ:氢氧化钠 猜想Ⅱ:碳酸钠 猜想Ⅲ:氢氧化钠和碳酸钠
【实验验证】
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入适量氯化钙溶液 | 产生白色沉淀 | 该反应的化学方程式为 Na2CO3+CaCl2=2NaCl+CaCO3↓ |
| (2)将上述反应后的混合物过滤取滤液加入 无色酚酞试液 | 无色变红色 | 证明猜想Ⅲ正确 |
【拓展应用】“氧气再生剂”的保存方法是密封存放干燥处.
