题目内容
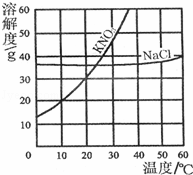
图为硝酸钾和氯化钠的溶解度曲线.由图可知:
(1)当温度为30℃时,硝酸钾的溶解度 (填“>”、“<”或“=”)氯化钠的溶解度.
(2)当硝酸钾中含有少量氯化钠时,可用 法提纯硝酸钾.
(3)硝酸钾、氯化钠都属于 (填“易溶”、“可溶”、“微溶”或“难溶”)物质.
(4)10℃时,将12g硝酸钾加入50g水中不断搅拌,形成溶液是 (填“饱和”或“不饱和”)溶液,溶液质量为 .
| 固体溶解度曲线及其作用;结晶的原理、方法及其应用;饱和溶液和不饱和溶液;物质的溶解性及影响溶解性的因素.. | |
| 专题: | 溶液、浊液与溶解度. |
| 分析: | 根据溶解度曲线的意义进行分析解答,依据溶解度曲线判断在某温度下物质溶解度的大小,根据溶解度和溶解性的关系分析解答即可. |
| 解答: | 解:(1)当温度为30℃时,硝酸钾的溶解度大于氯化钠的溶解度,故填:>. (2)硝酸钾的溶解度随温度的增大变化明显,当硝酸钾中含有少量氯化钠时,可用降温结晶法提纯硝酸钾,故填:降温结晶. (3)在20℃时,硝酸钾、氯化钠的溶解度都大于10g,都属于易溶物质,故填:易溶. (4)10℃时,硝酸钾的溶解度是20g,将12g硝酸钾加入50g水中不断搅拌,只能溶解10g硝酸钾,形成溶液是饱和溶液,溶液质量为50g+10g=60g,故填:饱和,60g |
| 点评: | 掌握溶解度的曲线的意义是正确解答本题的关键. |

 名校课堂系列答案
名校课堂系列答案稀土元素铕(Eu)是激光及原子能应用的重要材料.已知氯化铕的化学式为EuCl3,且铕元素在化合物中只有一种化合价,则氧化铕的化学式为( )
|
| A. | EuO | B. | Eu2O3 | C. | Eu3O2 | D. | EuO3 |
柑橘中含有对人体有益的柠檬烯.若用R表示柠檬烯,其完全燃烧的化学方程式为R+14O2 10CO2+8H2O,则柠檬烯的化学式为( )
10CO2+8H2O,则柠檬烯的化学式为( )
|
| A. | C5H10 | B. | C10H10 | C. | C10H16 | D. | C10H18 |
实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末.某兴趣小组的同学对该样品的成分及含量进行了探究.
【提出问题】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3.
则NaOH变质反应的化学方程式为 ;
【查阅资料】
碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
【实验探究】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入 ; | 白色沉淀产生 | 该反应的化学方程式为
|
| (2)将上述反应后的混合液过滤,取滤液加入 ; |
| 证明猜想Ⅱ成立. |
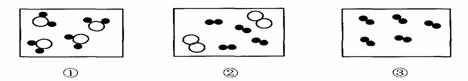
 下列分子的示意图中,“●”表示氢原子,“ ”表示氧原子。
下列分子的示意图中,“●”表示氢原子,“ ”表示氧原子。
 |
请根据上图回答下列问题:
(1)其中表示构成化合物的分子是图 (填编号),图 (填编号)中的分子构成的是混合物,图③中的分子的化学式是 。
(2)图①中的分子 (填“能”或“不能”)保持该物质的化学性质。
(3)写出图②中所示的物质转变成图①中所示物质的化学方程式 ________________________________________。
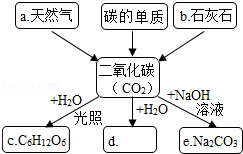
 于物理性质的是 ( )
于物理性质的是 ( )