题目内容
16.盐的分解反应可以分成不同的类别.现将盐的分解反应分成下列两类:第一类如CaC03、NH4HC03等的分解,第二类如KC1O3、KMn04等的分解.(1)将盐的分解反应分成上述两类的依据是第一类会生成二氧化碳,第二类会生成氧气;
(2)NaN03受热分解生成NaNO2和O2,写出该反应的化学方程2NaN03$\frac{\underline{\;\;△\;\;}}{\;}$2NaNO2+O2↑,该反应属于上述分类中的第二类(填“一”或“二”);
(3)某些盐也能发生和CaC03、NH4HC03类似的分解反应,试写出除了CaC03、NH4HC03以外的某种盐发生该类分解反应的化学方程2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
分析 (1)根据碳酸钙、碳酸氢铵受会生成二氧化碳,氯酸钾、高锰酸钾加热会生成氧气进行分析;
(2)根据硝酸钠在加热的条件下生成亚硝酸钠和氧气进行分析;
(3)根据碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳进行分析.
解答 解:(1)碳酸钙、碳酸氢铵受会生成二氧化碳,氯酸钾、高锰酸钾加热会生成氧气,所以将盐的分解反应分成上述两类的依据是第一类会生成二氧化碳,第二类会生成氧气;
(2)硝酸钠在加热的条件下生成亚硝酸钠和氧气,化学方程式为:2NaN03$\frac{\underline{\;\;△\;\;}}{\;}$2NaNO2+O2↑;
(3)碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳,化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
故答案为:(1)第一类会生成二氧化碳,第二类会生成氧气;
(2)2NaN03$\frac{\underline{\;\;△\;\;}}{\;}$2NaNO2+O2↑,二;
(3)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
点评 在解此类题时,首先分析应用的原理,然后找出反应物、生成物,最后结合方程式的书写规则书写方程式.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列实验现象的预测或分析中,错误的是( )
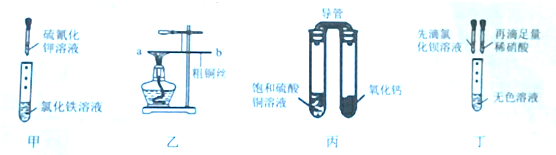

| A. | 实验甲:试管中溶液颜色变成红色 | |
| B. | 实验乙:系于细线下原来保持水平的粗铜丝,经过加热、冷却后b端略上升 | |
| C. | 实验丙:放置一段时间后,饱和硫酸铜溶液中出现蓝色晶体 | |
| D. | 实验丁:若出现白色沉淀且沉淀不消失,说明无色溶液中一定含硫酸根离子 |
1.将下列物质放入水中,可能得到无色透明溶液的一组是( )
| A. | Na2CO3、KCl、Na2SO4 | B. | K2SO4、BaCl2、HNO3 | ||
| C. | BaCl2、Na2CO3、AgNO3 | D. | FeCl3、CuSO4、NaOH |
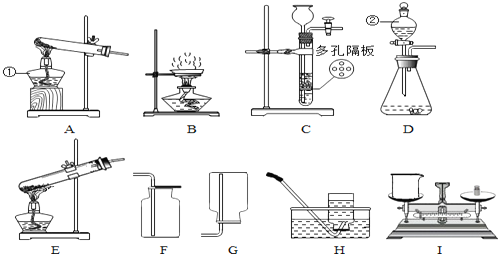
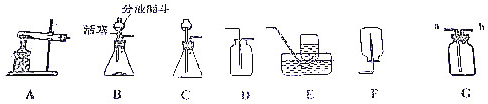
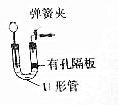 于排水法收集氧气,可在G中装满水后,将氧气从b口(“a”或“b”)进入.
于排水法收集氧气,可在G中装满水后,将氧气从b口(“a”或“b”)进入.