题目内容
5.草木灰是一种常见的农家肥料,其主要成分是碳酸钾(K2CO3);硫酸铵[(NH4)2SO4]是一种氮肥.为了给农民朋友提供技术指导,请对这两种肥料作相关性质探究.【查阅资料】:碳酸钾与纯碱具有相似的化学性质;
【实验探究】
| 探究过程 | K2CO3) | (NH4)2SO4 | 结论及化学方程式 |
| (1)分别取碳酸钾和硫酸铵固体,加入足量水溶解,取溶液分别滴入紫色石蕊溶液,观察溶液颜色变化 | 变蓝 | 变红 | 碳酸钾溶液显碱性 硫酸铵溶液显酸性 |
| (2)另取两种溶液分别加入足量 稀盐酸,观察现象 | 产生气泡 | 无明显现象 | 产生气泡的化学方程式 2HCl+K2CO3=2=KCl+CO2↑+H2O |
| (3)再取两种溶液分别加入Ba(OH)2溶液,观察现象 | 产生白色沉淀 | 有白色沉淀生成,同时以刺激性气味气体产生 | (NH4)2SO4与Ba(OH)2反应方程式 NH4)2SO4+Ba(OH)2═BaSO4↓+2H2O+2NH3↑ |
(4)某纯碱样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11g,加入到盛有50g稀盐酸的烧杯中,恰好完全反应,最后称得烧杯中溶液的质量为56.6g.计算:纯碱样品中碳酸钠的质量分数为多少?
分析 【实验探究】:①根据碳酸钾与纯碱具有相似的化学性质,呈碱性,使石蕊试液变蓝,硫酸铵呈酸性使石蕊试液变红;
②根据碳酸钾与盐酸反应生成氯化钾、水和二氧化碳解答;
③根据氢氧化钡和硫酸铵反应生成硫酸钡、氨气和水解答;
【交流共享】:②铵态氮肥和显碱性物质混合能生成氨气,从而降低肥效;
(4)根据质量守恒定律,反应前后减少的质量为二氧化碳的质量,利用二氧化碳纯碱样品中碳酸钠的质量.
解答 解:【实验探究】:①碳酸钾与纯碱具有相似的化学性质,所以碳酸钾溶液呈碱性,使石蕊试液变蓝,硫酸铵使石蕊试液变红,说明呈酸性,
②取两种溶液分别加入足量稀盐酸,碳酸钾与盐酸反应生成氯化钾、水和二氧化碳,反应的化学方程式为2HCl+K2CO3=2=KCl+CO2↑+H2O;
③氢氧化钡和硫酸铵反应生成硫酸钡、氨气和水,硫酸钡是不溶于水的白色物质,氨气有刺激性气味,
故填:产生白色沉淀、有刺激性气味的气体生成,(NH4)2SO4与 Ba(OH)2反应方程式为:NH4)2SO4+Ba(OH)2═BaSO4↓+2H2O+2NH3↑;
【讨论与反思】:②铵态氮肥和显碱性物质混合能生成氨气,从而降低肥效,
(4)生成二氧化碳的质量为11g+50g-56.6g=4.4g
设样品中碳酸钠的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
解得,x=10.6g
碳酸钠的质量分数=$\frac{10.6g}{11g}$×100%≈96.4%
答案:
| 探究过程 | K2CO3) | (NH4)2SO4 | 结论及化学方程式 |
| (1)分别取碳酸钾和硫酸铵固体,加入足量水溶解,取溶液分别滴入紫色石蕊溶液,观察溶液颜色变化 | 变蓝 | 变红 | 碳酸钾溶液显 碱性 硫酸铵溶液显酸性 |
| (2)另取两种溶液分别加入足量 稀盐酸,观察现象 | 产生气泡 | 无明显现象 | 产生气泡的化学方程式 2HCl+K2CO3=2=KCl+CO2↑+H2O |
| (3)再取两种溶液分别加入Ba(OH)2溶液,观察现象 | 产生白色沉淀 | 有白色沉淀生成,同时以刺激性气味气体产生 | (NH4)2SO4与Ba(OH)2反应方程式 NH4)2SO4+Ba(OH)2═BaSO4↓+2H2O+2NH3↑ |
(4)碳酸钠的质量分数为96.4%.
点评 本题主要考查氮肥、钾肥的判断和使用时的注意事项,难度稍大,须熟练运用酸碱盐的性质进行解答;

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案【查阅资料】洁厕灵主要含有盐酸,厕所污垢主要包括尿碱、水锈(主要成分为三氧化二铁)和油污等.
【提出猜想】
猜想1:含有氯化铜;猜想2:含有某种酸碱指示剂.
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样品加入过量氢氧化钠溶液,振荡 | 溶液颜色褪去,无蓝色沉淀生成 | 猜想1错误 |
| ②向①溶液中加入过量的稀盐酸,振荡 | 溶液颜色为蓝色 | 猜想2正确 |
(1)欲测定该洁厕灵的酸碱度,最适宜选用的是A(填字母);
A.pH试纸 B.酚酞溶液 C.紫色石蕊溶液
(2)写出该洁厕灵去除水锈时所发生反应的化学方程式:Fe2O3+6HCl═2FeCl3+3H2O;
(3)月月认为,不用碱溶液也能探究猜想1,她的实验方案为:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样,向样品中加铁片 | 产生大量气泡且无红色固体析出 | 猜想1错误 |
| A. | 烧杯 | B. | 托盘天平 | C. | 量筒 | D. | 玻璃棒 |
【实验】将一定量的稀盐酸加入到盛有饱和氢氧化钙溶液的烧杯中.
【提出问题】反应后溶液中溶质是什么?
【假设猜想】甲组同学的猜想如下,请在横线上写出猜想四.
猜想一:只有CaCl2
猜想二:有CaCl2和HCl
猜想三:有CaCl2、HCl和Ca(OH)2
猜想四:有CaCl2和Ca(OH)2.
【质疑】乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.
不合理的猜想是:猜想三,理由是盐酸和氢氧化钙不能共存.
【实验操作】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有Ca(OH)2.
(2)为了探究究竟是哪种猜想成立,丁组同学取适量反应后的溶液进行实验,选用了老师提供的pH试纸和一些溶液,依次进行一下两个实验,完成下列实验报告.
限选试剂:Ba(OH)2溶液、NaCl溶液、AgNO3溶液、Na2CO3溶液.
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1:用洁净干燥的玻璃棒蘸取溶液,粘在pH试纸上,与标准比色卡对照 | 试纸变色,溶液pH<7 | 溶液中有HCl |
| 步骤2:取少量反应后溶液于试管中,滴加碳酸钠溶液振荡 | 先产生气泡,后产生沉淀 | 溶液中有CaCl2 |
| A. | 氧分子:O2 | B. | 镁离子:$\stackrel{+2}{Mg}$ | C. | 2个氢原子:H2 | D. | 氧化铝:AlO |
 ”和“
”和“ ”分别表示氮原子和氧原子,如图2是氮气与氧气在放电条件下发生反应的微观模拟图,请回答下列问题:
”分别表示氮原子和氧原子,如图2是氮气与氧气在放电条件下发生反应的微观模拟图,请回答下列问题: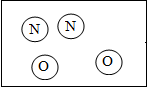 ,你的理论依据是反应前后原子种类、个数不变.
,你的理论依据是反应前后原子种类、个数不变.