题目内容
某化学小组用一蓝色混合溶液进行右图实验,已知该混合溶液中有AgNO3.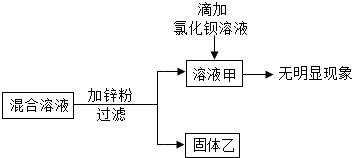
(1)实验后,溶液甲呈蓝色,向固体乙上滴加盐酸时 (填“有”或“没有”)气泡产生;固体乙中金属的成分是 .
(2)溶液甲中一定含有的溶质是: (写化学式).
(3)该实验过程中一定发生的反应的化学方程式为: .

(1)实验后,溶液甲呈蓝色,向固体乙上滴加盐酸时
(2)溶液甲中一定含有的溶质是:
(3)该实验过程中一定发生的反应的化学方程式为:
考点:盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:根据金属活动性顺序及其运用分析.排在氢之前的金属可与稀盐酸或稀硫酸反应产生氢气,排在前面的金属(除钾、钙、钠外)可将排在后面的金属从其盐溶液中置换出来结合实验的现象进行分析.
解答:解:实验后,溶液甲呈蓝色,说明含有铜盐,则锌粉不足,因此向固体乙上滴加盐酸时没有气泡产生;由金属活动性顺序及其运用可知,向AgNO3和铜盐混合溶液中加入锌粉,Zn应先与AgNO3反应后与Cu(NO3)2反应,由于锌粉量的不足,没有把硝酸铜溶液中的铜置换出来,因此溶液甲一定含有反应生成的Zn (NO3)2和剩余的Cu(NO3)2,可能含有AgNO3,滤渣中一定含有被置换出的银,可能含有铜,由以上分析可知,
(1)由于锌不足,因此向固体乙上滴加盐酸时没有气泡产生;固体乙中金属的成分是银 或者 银和铜;
(2)溶液甲中一定含有的溶质是Cu(NO3)2 Zn(NO3)2;
(3)该实验过程中一定发生的反应是锌和硝酸银反应产生硝酸锌和银,反应的方程式为:Zn+2AgNO3=Zn(NO3)2+2Ag;
故答案为:(1)没有; 银或者 银和铜;(2)Cu(NO3)2 Zn(NO3)2;(3)Zn+2AgNO3=Zn(NO3)2+2Ag.
(1)由于锌不足,因此向固体乙上滴加盐酸时没有气泡产生;固体乙中金属的成分是银 或者 银和铜;
(2)溶液甲中一定含有的溶质是Cu(NO3)2 Zn(NO3)2;
(3)该实验过程中一定发生的反应是锌和硝酸银反应产生硝酸锌和银,反应的方程式为:Zn+2AgNO3=Zn(NO3)2+2Ag;
故答案为:(1)没有; 银或者 银和铜;(2)Cu(NO3)2 Zn(NO3)2;(3)Zn+2AgNO3=Zn(NO3)2+2Ag.
点评:本题考查了金属活动性顺序的运用,主要考查了对金属活动性顺序的应用和理解,培养学生的应用能力和解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
重水的主要用途是在核反应堆中作减速剂,1个重水分子由2个重氢原子和1个氧原子构成,重氢原子核电荷数为1,相对原子质量为2.下列说法正确的是( )
| A、重水的相对分子质量为 20 |
| B、重氢原子核外有2个电子 |
| C、重氢分子的相对分子质量为 4 |
| D、重氢原子核内有2个质子 |
呼出的气体比空气中的气体含量多的是( )
| A、氮气 | B、氧气 |
| C、二氧化碳 | D、稀有气体 |