题目内容
17.下列图象能正确反映其对应关系的是( )| A. |  某温度下,向一定量接近饱和的硝酸钾溶液中不断加入过量的硝酸钾晶体 | |
| B. | 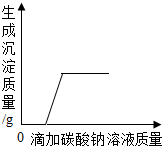 向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| C. | 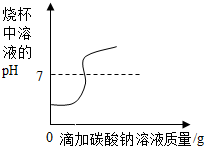 向氢氧化钠溶液中滴加过量的稀盐酸 | |
| D. | 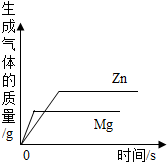 等质量的镁和锌同时分别放入两份溶质质量分数相同的足量稀盐酸中 |
分析 A、根据溶液达到饱和溶质质量分数不变解答;
B、根据碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳解答;
C、根据氢氧化钠溶液和盐酸溶液混合溶液pH的变哈解答;
D、根据等量的酸与足量金属反应产生氢气的质量相等解答.
解答 解:A、向一定量接近饱和的硝酸钾溶液中不断加入过量的硝酸钾晶则达到饱和以后溶液的溶质质量分数不再改变,故A错误;
B、向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量,则开始时盐酸与碳酸钠反应,没有沉淀产生,当盐酸耗尽则氯化钙与碳酸钠反应生成碳酸钙沉淀,故B正确;
C、氢氧化钠溶液显碱性,pH大于7,开始时pH应该大于7,故C错误;
D、金属与酸反应是氢气是来源于酸中的氢元素,因为两种金属过量,则酸会全部消耗,因为酸量相等,故生成氢气相等,故D错误.
故选B.
点评 此题是利用图示对常见的化学知识的考查,涉及的知识点较多,解题关键是如何分析相关的化学过程并读懂图象分析图象.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
17.某同学用氯化钠固体和蒸馏水配制氯化钠溶液,他往95毫升水(密度为1g/cm3)中加入5克氯化钠固体,配制成了实验需要的溶液,把溶液全部装入试剂瓶后,贴上标签,该标签的书写正确的是( )
| A. | 氯化钠溶液 100克 | B. | 氯化钠溶液 100mL | ||
| C. | 5%氯化钠溶液 100克 | D. | 5%氯化钠溶液 100mL |
12.下列各组物质在溶液中能大量共存且形成无色溶液的是( )
| A. | NaCl BaCO3 NaHCO3 | B. | KNO3 HCl CaCl2 | ||
| C. | H2SO4 FeCl3 NaNO3 | D. | NaOH ZnSO4 MgCl2 |
2.取一定量暴露在空气中且部分变质的碱石灰(NaOH与CaO的混合物),加水充分搅拌后过滤.下列选项中可能为所得滤液中溶质和滤渣成分的是( )
| 选项 | A | B | C | D |
| 滤液中的溶质 | NaOH、Ca(OH)2 | NaOH | NaOH、Na2CO3 | Na2CO3 |
| 滤渣 | CaCO3、Ca(OH)2 | Ca(OH)2 | CaCO3、Ca(OH)2 | CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
9.硝酸钾与氯化钾的溶解度曲线如图所示,下列说法正确的是( )
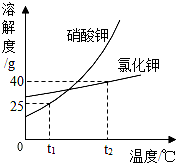

| A. | 从含有少量KCl的硝酸钾溶液中提纯KNO3应采取蒸发结晶法 | |
| B. | t2℃时,向100g水中加入50g氯化钾,充分溶解后,溶液的质量分数为33.3% | |
| C. | t2℃时,两物质的饱和溶液降温至t1℃,析出固体质量较多的是硝酸钾溶液 | |
| D. | 欲配制溶质的质量分数为20%的硝酸钾溶液,温度应不低于t1℃ |
6.在一定条件下,把一定质量的甲烷与氧气放入一密闭容器中充分反应,反应前后各物质质量如下
(1)其中待测值为2.8g,该反应的化学方程式为3CH4+5O2$\frac{\underline{\;点燃\;}}{\;}$2CO+CO2+6H2O
(2)若要使待测值为0,需要预先在容器里提高反应物中O2(填化学式)的量.
| 物质 | 甲烷 | 氧气 | X | 二氧化碳 | 水 |
| 反应前物质量(g) | 2.4 | 8 | 0 | 0 | 0 |
| 反应后物质量(g) | 0 | 0 | 待测 | 2.2 | 5.4 |
(2)若要使待测值为0,需要预先在容器里提高反应物中O2(填化学式)的量.
7.下列有关实验操作的描述中正确的是( )
| A. | 用pH试试测定洗衣粉水溶液的pH值时,若先用蒸馏水润湿试纸,再将溶液滴在试纸上,则测出的pH值比实际值大 | |
| B. | 用10mL规格的量筒量取6.5mL稀硫酸,某同学操作时仰视,则量出的硫酸少于6.5mL | |
| C. | 用托盘天平称量药品的质量时,若将药品与砝码的位置放错了,则一定会产生误差 | |
| D. | 取用细口瓶中的少量液体药品时,应将瓶上标签向着手心,并使瓶口与试管口紧挨缓慢倾倒 |