题目内容
3.将24g镁与铁的混合物投入足量稀盐酸中充分反应,生成气体的质量可能是( )| A. | 0.8g | B. | 1.6g | C. | 2.0g | D. | 2.4g |
分析 因为24g镁与铁的混合物,假设全是铁生成气体质量之间就是该题的答案.
解答 解:假设24g全是镁生成气体的质量为x
则Mg+2HCl═MgCl2+H2↑
24 2
24g x
$\frac{24}{24g}=\frac{2}{x}$ x=2g
假设24g全是铁生成气体的质量为y
Fe+2HCl═FeCl2+H2↑
56 2
24g y
$\frac{56}{24g}=\frac{2}{y}$ y≈0.86g
所以24g镁与铁的混合物投入足量稀盐酸反应生成气体的质量可能是1.6g,
故选B.
点评 本题主要考查学生利用化学方程式进行计算和分析的能力.解题的关键是分析两种金属都与足量的酸反应,生成氢气的质量关系.

练习册系列答案
相关题目
13.下列实验现象的描述错误的是( )
| A. | 白磷自燃产生大量的白烟 | |
| B. | 木炭在氧气中燃烧发出明亮白光 | |
| C. | 镁带在空气中燃烧发出耀眼的白光,生成白色固体氧化镁 | |
| D. | 硫磺在空气中燃烧,发出淡蓝色火焰,且有刺激性气味气体生成 |
11.汽油机是以汽油为燃料的一种内燃机,燃烧产物中含有大量对环境污染的物质.一种新型燃料的混合使用,使得上述问题有望得到缓解.已知一定量的新型燃料完全燃烧产生8.8克CO2和5.4克H2O,请判断该新型燃料可能是( )
| A. | CH3OH | B. | C2H5OH | C. | C6H12O6 |
15.下列实验操作符合安全要求的是( )
| A. | 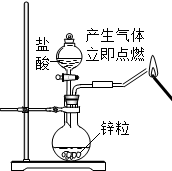 验证氢气的可燃性 | B. | 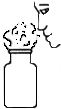 闻气体气味 | ||
| C. | 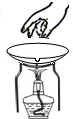 移走蒸发皿 | D. | 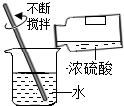 稀释浓硫酸 |
 化学元素与我们的健康是息息相关的,碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3),如图所示,超市销售的一种加碘盐标签上的部分文字说明.
化学元素与我们的健康是息息相关的,碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3),如图所示,超市销售的一种加碘盐标签上的部分文字说明. 如图是a、b、c三种固体物质溶解度曲线图,请回答:
如图是a、b、c三种固体物质溶解度曲线图,请回答: 如图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为钠盐,X,Y均为黑色粉末,D为红色金属单质,F在常温下为液态,回答下列问题.
如图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为钠盐,X,Y均为黑色粉末,D为红色金属单质,F在常温下为液态,回答下列问题. 济阳仁风镇是“中国西瓜之乡”,生产的富硒西瓜色泽好、糖分高、口感佳,被农业部认证为国家级“无公害产品”和“绿色食品”.
济阳仁风镇是“中国西瓜之乡”,生产的富硒西瓜色泽好、糖分高、口感佳,被农业部认证为国家级“无公害产品”和“绿色食品”.