题目内容
12.在一烧杯中盛有22.3g Na2CO3和NaCl组成的固体混合物,加足量水溶解,制成溶液.向其中逐渐滴加溶质质量分数为10%的稀盐酸73g,恰好完全反应.试通过计算求出反应后所得溶液中溶质的质量.分析 碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,由参加反应的稀盐酸的质量、溶质的质量分数,由反应的化学方程式列式计算出生成氯化钠的质量、参加反应的碳酸钠的质量,进而计算出反应后所得溶液中溶质的质量.
解答 解:设生成氯化钠的质量为x,参加反应的碳酸钠的质量为y,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117
y 73g×10% x
$\frac{73}{117}=\frac{73g×10%}{x}$ x=11.7g
$\frac{106}{73}=\frac{y}{73g×10%}$ y=10.6g
反应后所得溶液中溶质的质量为11.7g+22.3g-10.6g=23.4g.
答:反应后所得溶液中溶质的质量为23.4g.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.下列说法正确的是( )
| A. | 如果发现家里墙壁插座上的用电器起火,应立即用水浇灭 | |
| B. | 把锌棒放入有少量FeSO4的溶液中,锌棒质量减小 | |
| C. | 炒完菜后,及时擦掉锅底的水分,这样铁锅生锈速度加快 | |
| D. | 铁锅比铝锅传热快 |
3.下列实验现象的描述正确的是( )
| A. | 一氧化碳在空气中燃烧产生黄色火焰 | |
| B. | 磷在空气中燃烧生成五氧化二磷 | |
| C. | 硫在氧气中燃烧发出蓝紫色火焰,生成有刺激性气味的气体 | |
| D. | 木炭在氧气中燃烧,发出红光,生成大量的白色固体 |
4.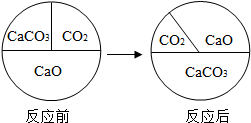 如图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是( )
如图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是( )
 如图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是( )
如图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是( )| A. | 该反应中CaO起催化作用 | B. | 该反应中CO2是生成物 | ||
| C. | 该反应是分解反应 | D. | 该反应是化合反应 |
8.下列判断正确的是( )
| A. | 将燃着的木条伸入充满某气体的集气瓶中,木条熄灭,则该气体一定是二氧化碳 | |
| B. | 二氧化碳有毒,空气中含量过高,会使人中毒死亡 | |
| C. | 某物质完全燃烧后生成二氧化碳和水,则该物质是由碳、氢、氧三种元素组成的 | |
| D. | 可用检验燃烧产物的方法鉴别氢气、一氧化碳 |