题目内容
15.为测定含有少量铜粉的氧化铜样品中氧化铜的质量分数,取样品10g,通入足量的CO并充分加热,待完全反应并冷却后,称得剩余固体的质量为8.4g,求该样品中氧化铜的质量分数是多少?分析 由10克到8.4克,前后减少的是参加反应的氧化铜中氧元素的质量,利用一氧化碳还原氧化铜的化学方程式,根据前后减少的质量差,即氧元素的质量可求出参加反应的氧化铜的质量,最后根据$\frac{氧化铜的质量}{混合物的质量}×100%$,即可求出氧化铜的质量占原有混合物的质量分数.
解答 解:设参加反应的氧化铜的质量为x
CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 CuO-Cu
80 64 80-64=16
x 10g-8.4g=1.6g
$\frac{80}{16}=\frac{x}{1.6g}$
x=8g
故氧化铜的质量分数为:$\frac{8g}{10g}×100%$=80%
答:该样品中氧化铜的质量分数是80%.
点评 本题是一道特殊的根据化学方程式的计算题,它不是根据某种具体物质的质量来求出另外一种物质的质量,而是根据两种具体物质的质量差来求出另一种物质的质量,只要把方法掌握好,和普通的根据化学方程式计算都是一样的.

练习册系列答案
相关题目
20.能证明某KNO3溶液在20℃时已达到饱和状态的方法是( )
| A. | 取少量该溶液,恒温20℃蒸发,有晶体析出 | |
| B. | 取少量该溶液,降温到10℃,有KNO3晶体析出 | |
| C. | 取少量该溶液升温,无KNO3晶体析出 | |
| D. | 温度不变时,向该溶液中加放少量KNO3晶体,晶体不再溶解 |
10.下列说法中符合质量守恒定律的是( )
| A. | 水结冰前后的质量保持不变 | |
| B. | 10毫升水与10毫升酒精混合后总体积小于20毫升 | |
| C. | 蜡烛完全燃烧后,生成水的质量和二氧化碳的质量等于蜡烛的质量 | |
| D. | 氯酸钾受热分解后,剩余固体的质量比原反应物的质量轻 |
4.下列离子可在同一溶液中大量共存的是( )
| A. | SO42-、H+、Na+、Cl- | B. | H+、SO42-、K+、CO32- | ||
| C. | Cl-、K+、Ca2+、NO3- | D. | Ca2+、CO32-、NO3-、Na+ |
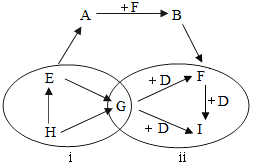 图中A~I表示几种初中化学常见的物质,“→”表示物质间存在相应的转化关系,部分反应物、生成物及反应条件已略去.已知圈i的转化均是分解反应.圈ii中的转化均是化合反应.D与G是常见的非金属单质,组成化合物E和H的元素种类相同.组成化合物F和I的元素种类也相同,A常用来中和土壤的酸性.
图中A~I表示几种初中化学常见的物质,“→”表示物质间存在相应的转化关系,部分反应物、生成物及反应条件已略去.已知圈i的转化均是分解反应.圈ii中的转化均是化合反应.D与G是常见的非金属单质,组成化合物E和H的元素种类相同.组成化合物F和I的元素种类也相同,A常用来中和土壤的酸性.
 已知A、B、C、D、E、F均为初中化学常见的物质.其中“-”表示相述的物质间能发生化学反应“→”表示转化,A和水反应转化为B,C在潮湿的空气中可以反应产生D,E为含有钠离子的一种盐,F可用硝酸银溶液和稀硝酸来检验,根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出)
已知A、B、C、D、E、F均为初中化学常见的物质.其中“-”表示相述的物质间能发生化学反应“→”表示转化,A和水反应转化为B,C在潮湿的空气中可以反应产生D,E为含有钠离子的一种盐,F可用硝酸银溶液和稀硝酸来检验,根据如图所示的转化关系,回答下列问题.(图中反应条件均已略去,反应物和产物均已给出)