题目内容
合成氨工业生产中所用的α﹣Fe催化剂的主要成分是FeO、Fe2O3.某合成氨工厂为使该催化剂催化活性更高而将90g FeO与200g Fe2O3混合.求:此时该催化剂中铁的质量分数?(要求写出计算过程,计算结果保留一位小数)
答案 分析:先计算出90g FeO与200g Fe2O3中的铁的总质量,然后由 ×100%进行计算.
×100%进行计算.
解:90g FeO中铁的质量是:90g×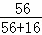 ×100%=70g,
×100%=70g,
200g Fe2O3中铁的质量是:200g×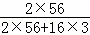 ×100%=140g,
×100%=140g,
则催化剂中铁的质量分数是: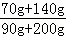 ×100%≈72.4%,
×100%≈72.4%,
答:此时该催化剂中铁的质量分数是72.4%.

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案金属是一种重要的材料,人类的生活和生产都离不开金属,全世界每年因生锈损失的钢铁,约占世界年产量的十分之一.
(1)兴趣小组的同学想探究钢铁锈蚀的条件,他将一个干净的铁钉放入试管中(如图一),定期观察并记录现象.图一中最先锈蚀的部位 (填写A、B或C);举出一种防止钢铁锈蚀的具体方法 ;
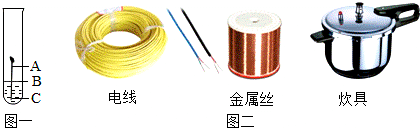
(2)根据图二的应用实例,试说出金属具有的一点物理性质 ;
(3)铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,原因是 ;
(4)下表中不同的金属被开发、利用的年代不同,决定这一先后顺序的关键因素是 ;
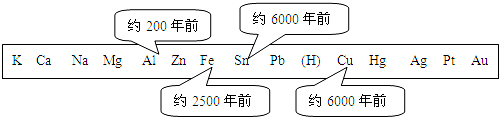
A.金属的活动性 B.金属的导电性
C.金属的延展性 D.地壳中金属元素的含量
(5)用质量相等的镁粉和铝粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应,产生氢气的质量和反应所用时间的关系如图三所示.则下列说法中正确的是 ;
A.曲线a、b分别表示镁、铝的反应情况
B.盐酸均反应完,镁恰好完全反应,铝剩余
C.盐酸均反应完,镁、铝也恰好完全反应
D.镁、铝都反应完,盐酸有剩余
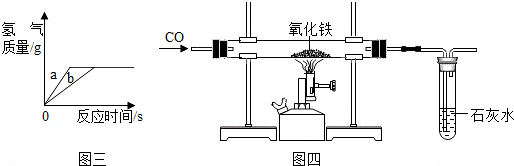
(6)联想到工业上用铁矿石冶炼铁,他们在实验室用CO还原氧化铁,实验如图四所示
①A、B处发生的现象分别是A 、B ;
②为了防止溶液倒吸,本实验停止加热前是否要先断开A和B的连接处? (填“需要”或“不需要”),理由是 气体会一直通到装置冷却,不会发生倒吸 .
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯和药品的质量/g | 166.5 | 166.3 | 166.1 | 166.1 |
(7)兴趣小组的同学又准确称取了11.5克生铁样品,放入装有100.0g稀硫酸(足量)的烧杯中(烧杯质量为55.0g).在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,
记录如表.求:①反应中产生氢气 克;②反应后所得溶液中溶质质量分数.(结果精确到0.1%)
实验室用 过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表:
过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表:
| 气体发生装置内物质的总质量/g | |
| 反应前 | 35.6 |
| 反应后 | 34.8 |
(1)反应中二氧化锰的作用是__________ ___________。
___________。
 (2)反应生成氧气的质量为_______________g(结果精确到0.1g,下同)。
(2)反应生成氧气的质量为_______________g(结果精确到0.1g,下同)。
(3)计算参加反应的过氧化氢的质量。
为了测定实验室中氯酸钾样品的纯度,某学习小组取2.5g该样品与0.5g二氧化锰混 合,加热该混合物t1时间后(假设杂质不参加反应),冷却,称量剩余固体的质量,重复以上操作,依次称得加热t1、t2、t3、t4时间后剩余固体的质量,记录
合,加热该混合物t1时间后(假设杂质不参加反应),冷却,称量剩余固体的质量,重复以上操作,依次称得加热t1、t2、t3、t4时间后剩余固体的质量,记录 数据如下表:
数据如下表:
|
| t1 | t2 | t3 | t4 |
| 剩余固体质量/g | 2.48 | 2.34 | 2.04 | 2.04 |
(1)在________时间后,该样品中的氯酸钾已经完全反应 (1分)
(2)完全反应后产生氧气的质量_______________ (1分)
(3)该样品中氯酸钾的质量分数 (4分)
 加热时 间
加热时 间