题目内容
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
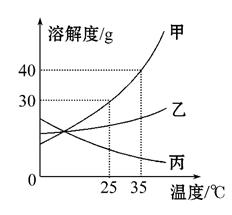
(1)25℃时,将25 g甲固体加入到50 g水中,充分溶解并恢复到原温度后,得到溶液的质量为 g。
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是 。
(3)现有操作步骤:a.溶解 b.过滤 c.降温结晶
d.加热浓缩。若甲固体中含有少量乙,则提纯甲的操作步骤是 (填字母序号)。
(4)将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数 (填“变大”“变小”或“不变”)。
(5)向100 g 35℃的水中加入45 g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出。你认为“全部溶解”的原因可能是
。
(1)25℃时,甲物质的 溶解度为30 g,即100 g水中最多溶解30 g,则50 g水中最多溶解15 g,所得溶液质量为15 g+50 g=65 g。(2)接近饱和的溶液变成饱和溶液,可通过加入溶质或蒸发溶剂的方法。(3)甲的溶解度受温度影响较大,而乙的溶解度受温度影响较小,故可通过降温结晶的方法提纯甲,具体步骤是:溶解,加热浓缩制成饱和溶液,再降温,析出晶体后过滤。(4)将35℃时丙的饱和溶液降温到25℃,丙的溶解度变大,溶液由饱和变为不饱和,没有晶体析出,故溶质质量分数不变。(5)甲的溶解度随温度的升高而增大,故开始发现甲全部溶解,一段时间后又有部分甲的晶体析出,说明开始时甲物质溶于水放热,温度升高,溶解度增大,冷却后溶液温度降低,溶解度变小,析出晶体。
溶解度为30 g,即100 g水中最多溶解30 g,则50 g水中最多溶解15 g,所得溶液质量为15 g+50 g=65 g。(2)接近饱和的溶液变成饱和溶液,可通过加入溶质或蒸发溶剂的方法。(3)甲的溶解度受温度影响较大,而乙的溶解度受温度影响较小,故可通过降温结晶的方法提纯甲,具体步骤是:溶解,加热浓缩制成饱和溶液,再降温,析出晶体后过滤。(4)将35℃时丙的饱和溶液降温到25℃,丙的溶解度变大,溶液由饱和变为不饱和,没有晶体析出,故溶质质量分数不变。(5)甲的溶解度随温度的升高而增大,故开始发现甲全部溶解,一段时间后又有部分甲的晶体析出,说明开始时甲物质溶于水放热,温度升高,溶解度增大,冷却后溶液温度降低,溶解度变小,析出晶体。
答案:(1)65 (2)加入甲物质(溶质)或恒温蒸发溶剂(水)
(3)adcb (4)不变 (5)甲固体溶于水时放热
【规律方法】
结晶法分两种方法,四种情况。两种方法是降温结晶法(冷却热饱和溶液法)和蒸发溶剂法,四种情况与两种方法的关系是:
(1)将溶解度受温度影响较大的固体溶质从其水溶液中析出(如将KNO3从其水溶液中析出)一般采用降温结晶(冷却热饱和溶液)的方法。
(2)将溶解度受温度影响不大的固体溶质从其水溶液中析出(如海水晒盐),一般采用蒸发溶剂的方 法。
法。
(3)溶解度受温度影响很大的固体中混有少量溶解度受温度影响较小的固体(如KNO3中混有NaCl),采用冷却热饱和溶液的方法分离。
(4)溶解度受温度影响不大的固体中混有少量溶解度受温度影响较大的固体(如NaCl中混有少量KNO3),采用蒸发溶剂的方法。

 ,量取所需水时,应选用的量筒的规格是 ▲ (填序号)① 50ml ② 100ml ③ 200ml
,量取所需水时,应选用的量筒的规格是 ▲ (填序号)① 50ml ② 100ml ③ 200ml  加反应,也不溶于水)求:(写出计算过程)
加反应,也不溶于水)求:(写出计算过程)
 ;
; 、
、 、
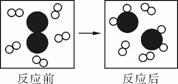
、 分别表示A、B、C三种不同的分子。则该反应的化学方程式中A、B、C前的化学计量数之比为( )。
分别表示A、B、C三种不同的分子。则该反应的化学方程式中A、B、C前的化学计量数之比为( )。