题目内容
7.街头出售氢气球的商贩常采取以下方法制备氢气:先在钢瓶内加入水、熟石灰和纯碱,再向钢瓶内加入少量铝制易拉罐碎片,即可产生氢气.以上操作产生H2的化学方程式为2Al+2NaOH+2X═2NaAlO2+3H2↑,则X的化学式为H2O;用化学方程式表示上述反应中出现氢氧化钠的原因为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.
根据碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,进行分析解答.
解答 解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2Al+2NaOH+2X═2NaAlO2+3H2↑,反应前铝、钠、氧、氢原子个数分别为2、2、2、2,反应后的生成物中铝、钠、氧、氢原子个数分别为2、2、4、6,根据反应前后原子种类、数目不变,则2X分子中含有4个氢原子和2个氧原子,则每个X分子由2个氢原子和1个氧原子构成,则物质X的化学式为H2O.
碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
故答案为:H2O;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
点评 本题难度不大,掌握利用化学反应前后原子守恒来确定物质的化学式的方法、盐的化学性质是正确解答此类题的关键.

练习册系列答案
相关题目
18.对实验室制取二氧化碳和用高锰酸钾制取氧气实验的比较,下列说法正确的是( )
| A. | 气体发生装置可能相同 | B. | 反应条件相同 | ||
| C. | 气体收集方法可能相同 | D. | 反应的基本反应类型相同 |
15.除去下列物质中的少量杂质,所用试剂或方法不正确的是( )
| 选项 | 物质 | 杂质 | 试剂或方法 |
| A | NaCl 固体 | 泥沙 | 加水溶解、过滤 |
| B | NaCl 溶液 | Na2CO3 | 滴加硫酸溶液至不再产生气泡 |
| C | KNO3溶液 | Ba(NO3)2 | 滴加适量K2SO4溶液、过滤 |
| D | N2 | O2 | 通过红热的铜丝 |
| A. | A | B. | B | C. | C | D. | D |
2.国外一本教材中把一种物质快速结合氧气生成氧化物的反应叫做燃烧反应,下列关于燃烧反应的说法不正确的是( )
| A. | 氢气爆炸属于燃烧反应 | B. | 化合反应一定是燃烧反应 | ||
| C. | 置换反应一定不是燃烧反应 | D. | 复分解反应不可能是燃烧反应 |
19.科学发现自然界中存在反粒子,它们跟普通粒子的质量、电量相等,而电性相反. 欧美科学家已经成功制造出反氢原子,这是人类探索反物质的一大进步,据此推测反氢原子的结构是( )
| A. | 由一个带正电荷的质子与一个带负电荷的电子构成 | |
| B. | 由一个带负电荷的质子与一个带正电荷的电子构成 | |
| C. | 由一个带正电荷的质子与一个带正电荷的电子构成 | |
| D. | 由一个带负电荷的质子与一个带负电荷的电子构成 |
17.下列关于“物质--用途--性质”的说法完全正确的是( )
| A. | 氧气--火箭发射--可燃性 | |
| B. | 干冰--制冷剂--与水反应吸热 | |
| C. | 氢氧化钠--改良酸性土壤--能与酸反应 | |
| D. | 一氧化碳--冶炼金属--还原性 |
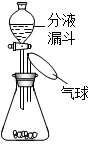 某化学小组设计了一组“吹气球”实验,装置如图所示,要使装置中的气球胀大,请写出分液漏斗和锥形瓶中的药品组合(三组).
某化学小组设计了一组“吹气球”实验,装置如图所示,要使装置中的气球胀大,请写出分液漏斗和锥形瓶中的药品组合(三组).