题目内容
完成细铁丝在氧气中燃烧的探究活动报告.
(1)探究活动的名称:探究铁丝在氧气中燃烧.
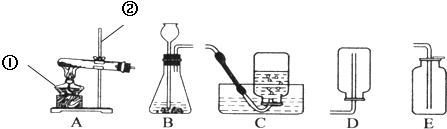
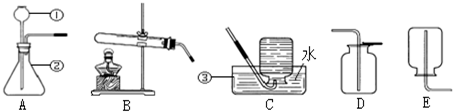
(2)实验所用仪器:集气瓶、 .
(3)操作步骤:
①先用砂纸将铁丝磨成光亮的银白色;②绕成螺旋状于一根火柴杆上;
③点燃火柴杆、将铁丝伸入盛有氧气的集气瓶中.火柴起 作用.
(4)反应的现象是 .
(5)该反应的化学方程式为 .
(6)问题分析:
①用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作原因可能 .
②某同学在实验时结果没有观察到细铁丝燃烧现象,实验失败的一种原因可能是 .
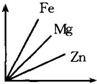
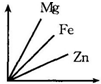
(7)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析完成下表:
通过以上实验,说明铁丝燃烧时出现火星的现象是由于 .
(1)探究活动的名称:探究铁丝在氧气中燃烧.
(2)实验所用仪器:集气瓶、
(3)操作步骤:
①先用砂纸将铁丝磨成光亮的银白色;②绕成螺旋状于一根火柴杆上;
③点燃火柴杆、将铁丝伸入盛有氧气的集气瓶中.火柴起
(4)反应的现象是
(5)该反应的化学方程式为
(6)问题分析:
①用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作原因可能
②某同学在实验时结果没有观察到细铁丝燃烧现象,实验失败的一种原因可能是
(7)小明对铁丝在氧气中燃烧为什么会火星四射进行探究.下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析完成下表:
| 物质 | 纯镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时的现象 | 剧烈燃烧,发出耀眼白光,无光星 | 剧烈燃烧极少火星 | 剧烈燃烧少量火星 |
考点:探究氧气的性质,书写化学方程式、文字表达式、电离方程式
专题:氧气、氢气的性质与用途
分析:根据已有的氧气的性质结合铁丝在氧气中燃烧的现象和有关的条件进行分析解答即可.
解答:解:(2)要探究铁丝在氧气中的燃烧,需要用到集气瓶和坩埚钳,故填:坩埚钳;
(3)③火柴杆在此起到了引燃的作用,故填:引燃;
(4)铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故填:剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体;
(5)铁在氧气中燃烧生成四氧化三铁,故填:3Fe+2O2
Fe3O4;
(6)①做细铁丝燃烧的实验时,发现瓶底炸裂,可能是瓶底没有放少量的水,故填:瓶底没有放少量的水;
②没有观察到细铁丝燃烧现象,可能是氧气的浓度太小,故填:氧气的浓度太小;
(7)根据表格提供的信息可以看出,当铁丝中含碳量达到较大量时产生火星,故含碳0.6%的铁丝燃烧会产生火星四射的现象,故填:剧烈燃烧,火星四射;铁丝中含有碳的量较高.
(3)③火柴杆在此起到了引燃的作用,故填:引燃;
(4)铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故填:剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体;
(5)铁在氧气中燃烧生成四氧化三铁,故填:3Fe+2O2
| ||
(6)①做细铁丝燃烧的实验时,发现瓶底炸裂,可能是瓶底没有放少量的水,故填:瓶底没有放少量的水;
②没有观察到细铁丝燃烧现象,可能是氧气的浓度太小,故填:氧气的浓度太小;
(7)根据表格提供的信息可以看出,当铁丝中含碳量达到较大量时产生火星,故含碳0.6%的铁丝燃烧会产生火星四射的现象,故填:剧烈燃烧,火星四射;铁丝中含有碳的量较高.
点评:本题考查的是铁在氧气中的燃烧的实验探究,完成此题,可以依据已有的知识结合题干提供的信息进行.

练习册系列答案
相关题目
下列实验装置或操作能达到实验目的是( )
A、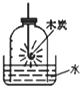 测定空气中氧气的体积分数 |
B、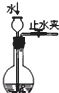 检查装置气密性 |
C、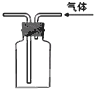 利用排空气法收集氧气 |
D、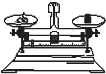 称量10.05克食盐 |
如图是氢氧化钠溶液与稀硫酸溶液恰好完全反应的微观示意图,由此得出的结论不正确的是( )

| A、反应结束时溶液的pH=7 |
| B、反应前后没有发生变化的微粒是Na+和SO42- |
| C、该反应是Na+和SO42-结合生成Na2SO4 |
| D、该反应的实质是H+和OH-结合生成H2O分子 |
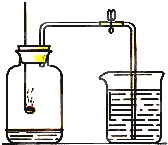 (1)空气中氧气体积含量的测定(如图)看到什么现象?得到什么结论?剩余的气体主要是什么气体?有什么性质?
(1)空气中氧气体积含量的测定(如图)看到什么现象?得到什么结论?剩余的气体主要是什么气体?有什么性质?