题目内容
暑假,同学们在帮老师整理实验室时,发现一瓶石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末.为了弄清白色粉末的成分及形成原因,他们进行了如下探究:
(1)对白色粉末成分的猜想和成因分析:
经过反复思考,同学们认为白色粉末还可能是
(2)设计实验:
甲同学取白色粉末装入试管中,加入足量的水、振荡.发现仍有白色固体不溶解.他们进行了如下实验,请完成如表实验报告:
(3)交流与反思
①通过上述实验的探究,同学们向实验室提出保存、使用液体药品时的下列建议,合理的是 (选填序号)
(A)密封保存 (B)使用前,临时配制 (C)禁止使用这种试剂
②实验室清洗装石灰水试剂瓶上的白色粉末时,可用稀盐酸,请写出其中有气泡产生的化学反应的文字表达式 .
(1)对白色粉末成分的猜想和成因分析:
| 白色粉末的成分 | 形成的原因 |
| 可能是CaCO3 | 石灰水与空气中CO2反应;化学反应的文字表达式为: |
| 可能是 | 暑假气温较高,水分蒸发,石灰水溶有的物质析出 |
(2)设计实验:
甲同学取白色粉末装入试管中,加入足量的水、振荡.发现仍有白色固体不溶解.他们进行了如下实验,请完成如表实验报告:
| 方案步骤 | 观察到的实验现象 | 结 论 |
| 取上述试管中的上层清夜,通入二氧化碳气体. | 上层清夜浑浊 | |
| 往上述试管中残留的固体中加入足量稀盐酸 | 有气泡产生 |
①通过上述实验的探究,同学们向实验室提出保存、使用液体药品时的下列建议,合理的是
(A)密封保存 (B)使用前,临时配制 (C)禁止使用这种试剂
②实验室清洗装石灰水试剂瓶上的白色粉末时,可用稀盐酸,请写出其中有气泡产生的化学反应的文字表达式
考点:实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据氢氧化钙能与二氧化碳反应生成碳酸钙沉淀,氢氧化钙溶液蒸发溶剂析出氢氧化钙分析白色粉末形成的原因.
(2)根据氢氧化钙微溶于水、溶液显碱性、碳酸钙能与盐酸反应生成气体分析.
(3)根据氢氧化钙的性质分析使用时的注意事项.
(2)根据氢氧化钙微溶于水、溶液显碱性、碳酸钙能与盐酸反应生成气体分析.
(3)根据氢氧化钙的性质分析使用时的注意事项.
解答:解:(1)氢氧化钙能与二氧化碳反应生成碳酸钙沉淀,反应的方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;由于氢氧化钙的溶解度随着气温的升高,溶质的溶解度会变小或溶剂蒸发,析出氢氧化钙粉末.所以,白色粉末可能是碳酸钙,也可能是氢氧化钙.
(2)由于氢氧化钙溶液能与二氧化碳反应生成碳酸钙,使溶液变浑浊,说明了溶液中含有含Ca(OH)2,由于碳酸钙能与盐酸反应生成气体,所以实验中产生气泡,则有碳酸钙.
(3)由于氢氧化钙的易与二氧化碳反应而变质.所以,氢氧化钙溶液要密封保存或使用前,临时配制.
清洗装石灰水试剂瓶上的白色粉末时,可用稀盐酸,是因为盐酸能与碳酸钙反应生成氯化钙、水和二氧化碳;
故答案为:(1)
CaCO3和Ca(OH)2
(2)
(3)AB,CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)由于氢氧化钙溶液能与二氧化碳反应生成碳酸钙,使溶液变浑浊,说明了溶液中含有含Ca(OH)2,由于碳酸钙能与盐酸反应生成气体,所以实验中产生气泡,则有碳酸钙.
(3)由于氢氧化钙的易与二氧化碳反应而变质.所以,氢氧化钙溶液要密封保存或使用前,临时配制.
清洗装石灰水试剂瓶上的白色粉末时,可用稀盐酸,是因为盐酸能与碳酸钙反应生成氯化钙、水和二氧化碳;
故答案为:(1)
| 白色粉末的成分 | 形成的原因 |
| 可能是CaCO3 | 石灰水与空气中CO2反应;化学反应的文字表达式为: Ca(OH)2+CO2=CaCO3↓+H2O |
| 可能是 Ca(OH)2 | 暑假气温较高,水分蒸发,石灰水溶有的物质析出 |
(2)
| 方案步骤 | 观察到的实验现象 | 结 论 |
| 取上述试管中的上层清夜,通入二氧化碳气体. | 上层清夜浑浊 | 白色粉末中有Ca(OH)2 |
| 往上述试管中残留的固体中加入足量稀盐酸 | 有气泡产生 | 白色粉末中含有CaCO3 |
点评:主要考查了氢氧化钙的变质,及氢氧化钙和碳酸钠的化学性质,培养学生分析问题、解决问题的能力.

练习册系列答案
相关题目
下列各组物质反应后,溶液的质量没有发生改变的是( )
| A、Cu(OH)2和稀硫酸 |
| B、碳酸钠固体和稀盐酸 |
| C、氧化铜和稀硫酸 |
| D、石灰水和稀盐酸 |
鉴别O2、CO、CO2三种气体,可行且简便的方法是( )
| A、将气体分别通入澄清石灰水 |
| B、将气体分别通入紫色石蕊溶液 |
| C、用燃着的木条分别伸入瓶内 |
| D、实验三种气体在水中的溶解性 |
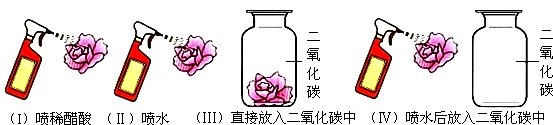
变量控制是设计对比实验的核心.在探究二氧化碳与水的反应中,某同学做了以下对比实验.取四朵用石蕊溶液染成紫色的干燥的小花.(Ⅰ)第一朵小花喷上稀醋酸.(Ⅱ)第二朵小花喷上水.(Ⅲ)第三朵小花直接放入盛满二氧化碳的集气瓶中.(Ⅳ)第四朵小花喷上水后,再放入盛满二氧化碳的集气瓶中.观察四朵花的颜色变化.关于该组实验设计的有关说法不准确的是( )

| A、实验Ⅱ、Ⅲ中紫花没有变色,说明水或者二氧化碳都不能使石蕊变色 |
| B、实验Ⅰ与实验Ⅳ中紫花变红,说明实验Ⅳ中生成了酸性物质 |
| C、实验Ⅰ与二氧化碳的性质无关,是辅助实验,证明了酸可以使紫色石蕊溶液变红 |
| D、这四组实验既证明了二氧化碳易溶于水,还证明了二氧化碳与水反应生成酸 |
下列基本操作是错误的是( )
| A、倾倒液体时,试剂瓶的标签应向着手心,以免药液腐蚀标签 |
| B、点燃酒精灯时要用火柴点燃 |
| C、药品不可直接放在托盘上称量 |
| D、用胶头滴管向试管中滴加液体时,应将滴管伸入试管内,以免药液滴在外面 |
 利用如图所示装置在实验室制取氧气:
利用如图所示装置在实验室制取氧气: