题目内容
9. 能源和环境成为人们日益关注的问题.目前煤炭在我国能源结构中占有的比例最大.
能源和环境成为人们日益关注的问题.目前煤炭在我国能源结构中占有的比例最大.(1)含硫煤燃烧会产生大气污染,其中二氧化硫排放到空气中会导致的环境问题是酸雨.
(2)为防治该污染,某工厂设计了新的治污方法,不仅吸收了二氧化硫,还得到了某种化工产品,该工艺流程如图所示:
Fe2(SO4)3和H2O吸收SO2生成FeSO4和H2SO4的化学方程式是Fe2(SO4)3+2H2O+SO2=2FeSO4+2H2SO4.
(3)为应对人们对能源和环保的需求,需要“节约现有能源、开发新能源、环保与发展共进”下列做法符合
该理念的有①③④(填序号).
①屋顶安装太阳能发电装置 ②焚烧田间秸秆,草木灰返田
③优化建筑设计,减少空调使用 ④乘坐轨道交通,减 少私家车使用.
分析 根据已有的知识进行分析解答,二氧化硫会形成酸雨,根据反应物和生成物书写反应的化学方程式;根据节能观点分析解答即可.
解答 解:(1)二氧化硫会与水反应生成亚硫酸,从而形成酸雨,故填:酸雨;
(2)Fe2(SO4)3和H2O吸收SO2生成FeSO4和H2SO4,该反应的化学方程式为Fe2(SO4)3+2H2O+SO2=2FeSO4+2H2SO4,故填:Fe2(SO4)3+2H2O+SO2=2FeSO4+2H2SO4;故填:Fe2(SO4)3+2H2O+SO2=2FeSO4+2H2SO4;
(3))①屋顶安装太阳能发电装置能节约能源,正确;
②焚烧田间秸秆,草木灰返田会造成环境污染,错误;
③优化建筑设计,减少空调使用可以节约能源,正确;
④乘坐轨道交通,减少私家车使用可以节约能源保护环境,正确;
故填:①③④.
点评 本题考查的是化学与环境的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
17.如图是甲、乙、丙三种物质的溶解度曲线.下列判断不正确的是( )


| A. | T2℃丙的饱和溶液温度降低变为不饱和溶液 | |
| B. | 三种物质中,溶解度随温度变化最明显的是甲 | |
| C. | T2℃甲的饱和溶液温度降低,溶质的质量分数减小 | |
| D. | 甲和乙的饱和溶液分别由T2℃降到T1℃,甲析出晶体的质量比乙的多 |
4.对如表所示日常生活中的现象解释不合理的是( )
| 生活中的现象 | 解 释 | |
| A | 墙内开花墙外香 | 分子在不断运动 |
| B | 乙醇、油漆需要密闭保存 | 分子质量很小,故液体均易挥发 |
| C | 湿衣服在阳光下比阴凉处干得快 | 温度升高,分子运动速度加快 |
| D | 石油气加压可贮存在钢瓶中 | 分子间有间隔,加压使得间隔缩小 |
| A. | A | B. | B | C. | C | D. | D |
14.某同学想用实验证明FeCl3溶液显黄色不是Cl-离子造成的,下列实验无意义的是( )
| A. | 加水稀释后FeCl3溶液黄色变浅 | |
| B. | 向FeCl3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失 | |
| C. | 向FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失 | |
| D. | 观察KCl溶液没有颜色 |

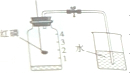 如图所示,测定空气中氧气含量实验的反应原理是(用文字或符号表达式表示)磷+氧气$\stackrel{点燃}{→}$五氧化二磷,对反应物的要求是消耗掉氧气,且不生成气体,实验中的注意事项是足量的红磷、装置的气密性良好、装置冷却至室温再打开止水夹(至少写三点).实验后所得剩余气体具有不燃烧,不支持燃烧,难溶于水(写出三点)的性质.
如图所示,测定空气中氧气含量实验的反应原理是(用文字或符号表达式表示)磷+氧气$\stackrel{点燃}{→}$五氧化二磷,对反应物的要求是消耗掉氧气,且不生成气体,实验中的注意事项是足量的红磷、装置的气密性良好、装置冷却至室温再打开止水夹(至少写三点).实验后所得剩余气体具有不燃烧,不支持燃烧,难溶于水(写出三点)的性质.