题目内容
5.二氧化氯(ClO2)可用于自来水消毒.以粗盐为原料生产ClO2的工艺主要包括:①粗盐精制;②特殊条件下电解NaCl溶液制NaClO3;③ClO2的制取.工艺流程如图,其中反应Ⅲ制取ClO2的化学方程式为2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O.
关于该实验的下列说法不正确的是( )
| A. | 过量的X是碳酸钠溶液、物质Y可循环利用 | |
| B. | 操作A的名称是过滤,用到的玻璃仪器有玻璃棒、漏斗、烧杯 | |
| C. | 反应Ⅱ的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | |
| D. | 为提高经济效益,生产过程中可将H2和Cl2制成HCl充分利用 |
分析 A、根据试剂X是为了除去氯化钙又不能引入新的杂质,以及2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O进行分析;
B、根据操作A是除去液体中的不溶性固体的操作进行分析;
C、根据反应Ⅱ中生成NaClO3和氢气,因此Ⅱ中反应的化学方程式为:NaCl+3H2O$\frac{\underline{\;通电\;}}{\;}$NaClO3+3H2↑进行分析;
D、根据氢气和氯气在点燃的条件下会生成氯化氢气体进行分析.
解答 解:A、试剂X是为了除去氯化钙又不能引入新的杂质,所以试剂X是碳酸钠,通过分析2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O可知,Y是氯化钠,可以循环使用,故A正确;
B、操作A是除去液体中的不溶性固体的操作,所以操作A的名称是过滤,用到的玻璃仪器有玻璃棒、漏斗、烧杯,故B正确;
C、反应Ⅱ中生成NaClO3和氢气,因此Ⅱ中反应的化学方程式为:NaCl+3H2O$\frac{\underline{\;通电\;}}{\;}$NaClO3+3H2↑,故C错误;
D、氢气和氯气在点燃的条件下会生成氯化氢气体,故D正确.
故选:C.
点评 本题以工业上用NaCl还原NaClO3生产ClO2的工艺流程考查混合物的分离、提纯,明确流程是解答本题的关键,注意发生的化学反应来解答,题目难度较大.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
1.除去下列各物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是( )
| 选项 | 物质 | 杂质 | 除杂试剂及操作方法 |
| A | 二氧化碳 | 一氧化碳 | 通入氧气,点燃 |
| B | 氯化钾溶液 | 碳酸钾 | 加入过量氯化钙溶液,充分反应后过滤 |
| C | 锌粉 | 铁粉 | 加入适量氯化锌溶液,充分反应后过滤 |
| D | 氢气 | 氯化氢 | 先通过过量氢氧化钠溶液,再通过过量浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
20.小林对下列符合中数字含义的理解正确的是( )
| A. | S2+:一个硫离子带2个单位正电荷 | |
| B. | Mn2+:锰元素的化合价为+2价 | |
| C. | NH3:该物质中N、H元素的个数比为1:3 | |
| D. | O2:2个氧原子 |
10.奠定近代化学基础的是( )
| A. | 门捷列夫发现元素周期律 | |
| B. | 火的发现和利用使人类变聪明、强大 | |
| C. | 道尔顿和阿伏伽德罗得出的原子论和分子学说 | |
| D. | 绿色化学 |

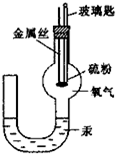 如图所示,在玻璃燃烧匙中盛有一定量硫粉,金属丝用于加热(不和硫反应),球形容器内充满氧气,U形管内盛液态汞.反应前,两侧液面持平.给金属丝通电加热,使硫与容器中的氧气发生反应,此时,可以观察到U形管中水银柱左边高于右边.反应结束后,静置片刻,使容器内的温度恢复到反应前的温度.此时,可观察到U形管两侧的水银柱液面仍持平.(相同条件下,气体分子数相同则气体的体积相同)2请回答下列问题:
如图所示,在玻璃燃烧匙中盛有一定量硫粉,金属丝用于加热(不和硫反应),球形容器内充满氧气,U形管内盛液态汞.反应前,两侧液面持平.给金属丝通电加热,使硫与容器中的氧气发生反应,此时,可以观察到U形管中水银柱左边高于右边.反应结束后,静置片刻,使容器内的温度恢复到反应前的温度.此时,可观察到U形管两侧的水银柱液面仍持平.(相同条件下,气体分子数相同则气体的体积相同)2请回答下列问题: