题目内容
为防止碘缺乏病采取的有效措施是食盐“加碘”.市场上销售的“加碘食盐”,是在食盐中加入了少量的碘酸钾(KIO3),
(1)“加碘食盐”为人体补充的是 (填“碘元素”或“碘单质”).
(2)计算碘酸钾的相对分子质量为 .
(3)碘酸钾中碘元素的质量分数是 (计算结果保留到0.1%).
(4)若一个人一天从食盐中摄入的碘酸钾的质量为42.8mg,则进入人体的碘元素是 mg(计算结果保留到0.1mg).
(1)“加碘食盐”为人体补充的是
(2)计算碘酸钾的相对分子质量为
(3)碘酸钾中碘元素的质量分数是
(4)若一个人一天从食盐中摄入的碘酸钾的质量为42.8mg,则进入人体的碘元素是
考点:相对分子质量的概念及其计算,元素的概念,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据物质的组成常用元素来描述分析回答.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据化合物中元素的质量分数=
×100%,进行分析解答.
(4)根据碘酸钾中碘元素的质量分数计算进入人体的碘元素的质量.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
(4)根据碘酸钾中碘元素的质量分数计算进入人体的碘元素的质量.
解答:解:(1)“加碘食盐”中的“碘”不是以单质、分子、原子等形式存在,这里所指的“碘”是强调存在的元素,与具体形态无关.
(2)碘酸钾的相对分子质量=39+127+16×3=214.
(3)碘酸钾中碘元素的质量分数是=
×100%=
×100%=59.3%.
(4)若一个人一天从食盐中摄入的碘酸钾的质量为42.8mg,进入人体的碘元素的质量为:42.8mg×59.3%=25.4mg.
故答案为:(1)碘元素;(2)214;(3)59.3%.(4)25.4.
(2)碘酸钾的相对分子质量=39+127+16×3=214.
(3)碘酸钾中碘元素的质量分数是=
| 相对原子质量×原子个数 |
| 相对分子质量 |
| 127 |
| 214 |
(4)若一个人一天从食盐中摄入的碘酸钾的质量为42.8mg,进入人体的碘元素的质量为:42.8mg×59.3%=25.4mg.
故答案为:(1)碘元素;(2)214;(3)59.3%.(4)25.4.
点评:本题难度不大,主要考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图表示治理汽车尾气所涉及反应的微观过程.下列说法正确的是( )
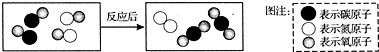

| A、图中单质的化学式为N2 |
| B、该反应使有害气体转化为无害气体 |
| C、该反应属于化合反应 |
| D、该反应分子个数发生了改变,不符合质量守恒定律 |
 代表硫原子)
代表硫原子)