题目内容
实验室常利用以下装置完成气体制备及性质实验.请回答:
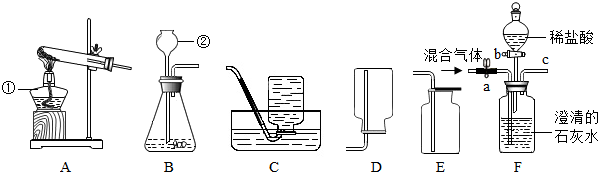
(1)指出编号仪器的名称:② .
(2)以上 (从A-E中选择)装置有一处明显的错误,请加以改正 .利用改正后的装置继续完成后面的实验.
(3)使用高锰酸钾制取氧气,反应原理用化学方程式表示为 ;为防止高锰酸钾粉末进入导管,应采取的措施是 .欲收集较纯净的氧气应选择收集装置 (填序号).
(4)若要分离CO2和CO的混合气体,可将气体通过F装置(液体药品均足量),实验开始时关闭活塞 ,打开活塞 ,此时从导管c逸出的气体主要是 .一段时间后,经过相关操作,将分液漏斗中的稀盐酸滴入广口瓶中,此时发生的化学反应的化学方程式为 .

(1)指出编号仪器的名称:②
(2)以上
(3)使用高锰酸钾制取氧气,反应原理用化学方程式表示为
(4)若要分离CO2和CO的混合气体,可将气体通过F装置(液体药品均足量),实验开始时关闭活塞
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的化学性质,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热,加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的气体比较纯净.实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.若要分离CO2和CO的混合气体,可将气体通过F装置,实验开始时关闭活塞b,打开活塞a,此时从导管c逸出的气体主要是一氧化碳;一段时间后,关闭活塞a,打开活塞b,将分液漏斗中的稀盐酸滴入广口瓶中,发生的反应是碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,配平即可.
解答:解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)A装置有一点错误之处,改正为:导管只能露出橡皮塞一点;故答案为:A;导管只能露出橡皮塞一点;
(3)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的气体比较纯净;故答案为:2KMnO4
K2MnO4+MnO2+O2↑;在试管口放一团棉花;C;
(4)若要分离CO2和CO的混合气体,可将气体通过F装置,实验开始时关闭活塞b,打开活塞a,此时从导管c逸出的气体主要是一氧化碳;一段时间后,关闭活塞a,打开活塞b,将分液漏斗中的稀盐酸滴入广口瓶中,发生的反应是碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,配平即可;故答案为:b;a;CO;CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)A装置有一点错误之处,改正为:导管只能露出橡皮塞一点;故答案为:A;导管只能露出橡皮塞一点;
(3)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的气体比较纯净;故答案为:2KMnO4
| ||
(4)若要分离CO2和CO的混合气体,可将气体通过F装置,实验开始时关闭活塞b,打开活塞a,此时从导管c逸出的气体主要是一氧化碳;一段时间后,关闭活塞a,打开活塞b,将分液漏斗中的稀盐酸滴入广口瓶中,发生的反应是碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,配平即可;故答案为:b;a;CO;CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
在一定环境中,常温常压下的水可以瞬间结成冰,俗称“热冰”.下列说法正确的是( )
| A、结成“热冰”后,分子停止运动 |
| B、“热冰”在任何条件下都不会熔化 |
| C、“热冰”与水的化学性质不同 |
| D、“热冰”是纯净物 |
下列物质不是按单质、化合物、氧化物、混合物分类的是( )
| A、液态氧 稀盐酸 氧化铁 空气 |
| B、硫磺 甲烷 氧化钙 煤 |
| C、水银 氯酸钾 氧化铜 合金 |
| D、氖气 碳酸钙 氧化铝 矿泉水 |

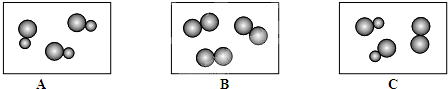
 ”、“
”、“ ”表示不同元素的原子,请用序号填空:
”表示不同元素的原子,请用序号填空: