题目内容
14.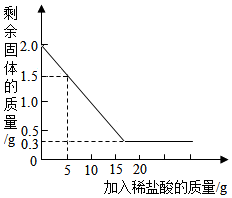 某石灰厂有一批石灰石原料,其中含有的杂质为二氧化硅(二氧化硅不溶于水,不与盐酸反应.高温时比发生分解)为了测定该石灰石的纯度,兴趣小组的同学取用2g这种石灰石样品,用实验室未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后,根据每次稀盐酸用量及剩余固体质量和实验数据绘制成图象(如图).计算:
某石灰厂有一批石灰石原料,其中含有的杂质为二氧化硅(二氧化硅不溶于水,不与盐酸反应.高温时比发生分解)为了测定该石灰石的纯度,兴趣小组的同学取用2g这种石灰石样品,用实验室未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后,根据每次稀盐酸用量及剩余固体质量和实验数据绘制成图象(如图).计算:| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5克 | 1.5克 |
| 第二次加入5克 | 1.0g |
| 第三次加入5克 | 0.5克 |
| 第四次加入5克 | 0.3克 |
( 2 )该石灰石样品中含碳酸钙的质量是1.7克;
(3)所用稀盐酸的溶质质量分数是多少?
分析 由表中数据可知,第二次反应的碳酸钙质量是0.5g,前三次中的稀盐酸完全反应,因此根据前三次中任一次的数据可以计算所用稀盐酸中溶质的质量分数.
解答 解:(1)分析上述图与表,第二次加入稀盐酸后,剩余固体的质量是1.0g.故填:1.0.
(2)该石灰石样品中碳酸钙的质量为:2g-0.3g=1.7g;故填:1.7.
(3)设5g稀盐酸中溶质的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑,
100 73
0.5g x
$\frac{100}{73}=\frac{0.5g}{x}$ 解得:x=0.365g,
所用稀盐酸中溶质的质量分数为:$\frac{0.365g}{5g}$×100%=7.3%,
答:稀盐酸的质量分数为7.3%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析表中数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
6.按溶解、过滤、蒸发的操作顺序,可将下列各组物质分离的一组是( )
| A. | 铜粉和铁粉 | B. | 食盐和泥沙 | C. | 水和酒精 | D. | 水和牛奶 |
3.实验室用如图所示装置制取气体,下列实验操作正确的是( )
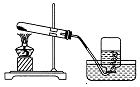

| A. | 加热前,将集气瓶注满水,用玻璃片盖好倒立水槽中 | |
| B. | 开始收集时先将导管口移入集气瓶口,再开始加热 | |
| C. | 集满气体后,将集气瓶移出水槽,再盖上玻璃片 | |
| D. | 停止加热时,要先熄灭酒精灯,再将导管移出水槽 |
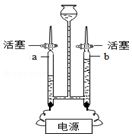 用如图装置进行水的电解实验:
用如图装置进行水的电解实验: 有下列四个化学反应:(反应条件已省略)
有下列四个化学反应:(反应条件已省略)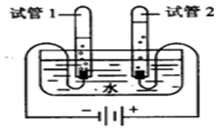 小刚利用如图所示的装置探究水的组成.通电一段时间后,试管1中所收集的气体为氢气,具有助燃性的气体存在于试管2(填“试管1”或者“试管2”),检验方法是将带火星的木条伸入试管,木条复燃,证明该气体为氧气;此实验说明水由氢元素和氧元素组成的.
小刚利用如图所示的装置探究水的组成.通电一段时间后,试管1中所收集的气体为氢气,具有助燃性的气体存在于试管2(填“试管1”或者“试管2”),检验方法是将带火星的木条伸入试管,木条复燃,证明该气体为氧气;此实验说明水由氢元素和氧元素组成的.