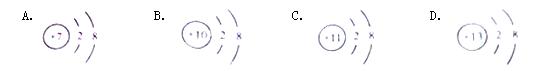题目内容
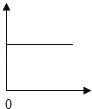
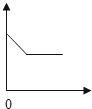
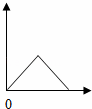
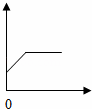
实验室常用二氧化锰与氯酸钾共热制氧气,表示混合物中二氧化锰的质量分数随反应间的变化图象(横坐标表示时间、纵坐标表示混合物中二氧化锰的质量分数)是( )
|
| A. |
| B. |
| C. |
| D. |
|
| 催化剂的特点与催化作用.. | |
| 专题: | 元素化合物知识型. |
| 分析: | 混合物中二氧化锰的质量分数= A、混合物中的氯酸钾不断减少,所以二氧化锰的质量分数不会一成不变; B、混合物中的氯酸钾不断减少,所以二氧化锰的质量分数不会降低; C、反应前混合物中就有一定量的二氧化锰,所以质量分数不能从0点开始; D、混合物中的氯酸钾不断减少,所以二氧化锰的质量分数会先增大,增大到一定程度也会不再增大. |
| 解答: | 解:混合物中二氧化锰的质量分= 故选D |
| 点评: | 记住催化剂的“一改变,二不变”的特性,即“改变化学反应的速率;反应前后,自身的质量和化学性质都不改变”,是解答本题的关键. |

用量筒量取液体时,某同学操作如下:俯视液体凹液面最低处读数为30mL,倒出部分液体后,又仰视凹液面最低处读数为20mL.则取出液体的实际体积为( )
|
| A. | 10mL | B. | 大于10mL | C. | 小于10mL | D. | 无法判断 |
下列化学符号中,表示2个氢分子的是( )
|
| A. | H2 | B. | 2H | C. | 2H2 | D. | 2H+ |
小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开研究:
第一组实验:取5支集气瓶,编号为①、②、③、④、⑤,分别装入其总体积10%、20%、30%、40%、50%上的水.用排水法收集氧气,恰好把5只集气瓶中的水排去.将带火星的木条依次插入①~⑤号瓶中,记录实验现象.
小亮在前组实验的基础上又做了第二组和第三组实验,三组实验的数据和现象见下表.
| 第一组 | 第二组 | 第三组 | |||||||||
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的O2占容积的体积分数(%) | 10 | 20 | 30 | 40 | 50 | 31 | 33 | 35 | 37 | 39 | 34 |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
根据实验回答下列问题:
(1)写出一个实验室制取氧气的符号表达式: .
(2)使用带火星的木条验满氧气的方法是否可靠: (填“是”或“否”).
(3)集气瓶中氧气的体积分数=收集的氧气占容积的体积分数+瓶中空气占容积的体积分数× %.
(4)收集的氧气占容积的体积分数最低为 %时,可使带火星的木条复燃,这时集气瓶中氧气的体积分数是 %(计算结果保留整数).
 ×100%,根据二氧化锰的质量和反应混合物的质量的变化情况进行分析.
×100%,根据二氧化锰的质量和反应混合物的质量的变化情况进行分析. ×100%,二氧化锰是该反应的催化剂,反应前后质量不变,过氧化氢会分解生成氧气,反应混合物的质量会减小,所以混合物中二氧化锰的质量分会越来越大,因反应前混合物中就有一定量的二氧化锰,所以质量分数不能从0点开始,因过氧化氢分解完后反应混合物的质量将不再减小,所以增大到一定程度也会不再增大.
×100%,二氧化锰是该反应的催化剂,反应前后质量不变,过氧化氢会分解生成氧气,反应混合物的质量会减小,所以混合物中二氧化锰的质量分会越来越大,因反应前混合物中就有一定量的二氧化锰,所以质量分数不能从0点开始,因过氧化氢分解完后反应混合物的质量将不再减小,所以增大到一定程度也会不再增大.