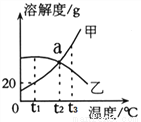
题目内容
工业上常用电解饱和食盐水的方法得到所需要的原料。化学反应的方程式如下:
2NaCl+2H2O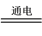 2NaOH+X↑+H2↑。则X的化学式为
2NaOH+X↑+H2↑。则X的化学式为
A. HCl B. HClO C. O2 D. Cl2
 阅读快车系列答案
阅读快车系列答案实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验。
查阅资料:烧碱固体有吸水性且能与二氧化碳发生反应。
无水硫酸铜遇水会由白色变成蓝色。
①制备氧化铜并检验产物,装置如图所示(省略夹持仪器):
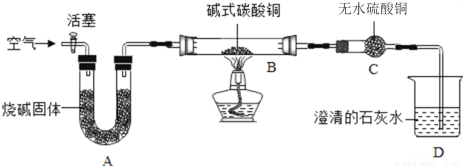
步骤一:连接A和B,打开活塞,通入空气。
步骤二:关闭活塞,连上C和D开始加热。观察到C中固体变蓝,D中澄清石灰水变浑浊。
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热。
加热时间(min) | 0 | t1 | t2 | t3 |
B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
①B中发生反应的化学方程式为:__________ , A的作用是吸收空气中的_______ ,防止对产物检验造成干扰。选择t3时停止加热的理由是____________。
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图所示:写出该反应的化学方程式________,实验过程中,观察到F中溶液变浑浊,E中的现象是___________ 反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是____________

③若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因______________。
④计算②反应后理论上可制得多少克铜__________。
FeCl3溶液能对过氧化氢溶液的分解起催化作用。某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响。
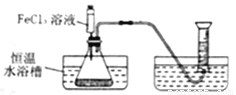
写出本实验发生反应的符号表达式_______;
I.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,如图观察到____________,就可以粗略判断,得出实验结果。为进一步判断上述实验结论的准确性,运用上图,小刚同学进行了如下实验方案设计。
II.[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间。
[方案二]在不同过氧化氢溶液下,测定______________;
方案二的实验测量结果:
实验序号 物理量 | 30%H2O2溶液的体积(mL) | 2%FeCl3溶液的体积(mL) | 加入H2O的体积(mL) | 反应的时间(min) | 生成O2的体积(mL) |
1 | 5 | x | 20 | 5 | V1 |
2 | 10 | 3 | 15 | y | V2 |
表中x=___________,y=_____________;
实验结论:通过测量,若V1______V2(填“>”、“=”或“<”),说明___。