题目内容
80g SO3和64g SO2所含的硫元素的质量比为 .
考点:化合物中某元素的质量计算
专题:化学式的计算
分析:根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:80g SO3和64g SO2所含的硫元素的质量比为(80g×
×100%):(64g×
×100%)=1:1.
故答案为:1:1.
| 32 |
| 32+16×3 |
| 32 |
| 32+16×2 |
故答案为:1:1.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
一氧化氮是一种难溶于水的气体,其密度比空气略大,且很易与空气中的氧气反应,则一氧化氮的收集方法是( )
| A、向下排空气法 |
| B、向上排空气法 |
| C、向上排空气法和排水法 |
| D、排水法 |
在60℃恒温条件下,取200g A物质的溶液蒸发掉20g水后,析出10g A的无水晶体,再蒸发掉20g水后,又析出20g A的无水晶体,则原溶液中溶质的质量分数为( )
| A、64.4% |
| B、50.0% |
| C、47.5% |
| D、33.3% |
下列实验现象的描述中,不正确的是( )
| A、木炭在氧气中燃烧发出白光 |
| B、铁丝在氧气中燃烧火星四射,生成黑色固体 |
| C、硫在空气中燃烧发出淡蓝色火焰 |
| D、红磷在氧气中燃烧冒出大量白雾 |
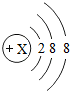 则:X的值是
则:X的值是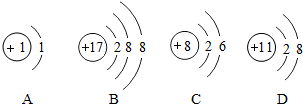
 水是生命之源,请用所学知识回答有关水的问题.
水是生命之源,请用所学知识回答有关水的问题.