题目内容
8.工业上常用NaOH溶液处理铝土矿(主要成分Al2O3),反应的化学方程式Al2O3+2NaOH═2NaAlO2+H2O.现对204t含Al2O3 80%的某种铝土矿进行处理(杂质不参与反应),理论上需要消耗溶质质量分数为50%的NaOH溶液多少?分析 根据Al2O3与NaOH反应的化学方程式,由氧化铝的质量可以计算氢氧化钠溶液的质量.
解答 解:设需要消耗NaOH溶液的质量为x,
Al2O3+2NaOH=2NaAlO2+H2O
102 80
204t×80% x×50%
$\frac{102}{204t×80%}$=$\frac{80}{x×50%}$
x=256t
答:理论上需要消耗溶质质量分数为50%的NaOH溶液256t.
点评 本题考查的是有关化学方程式的计算问题,考查内容简单注重基础,需熟练掌握计算步骤和格式即可解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列物质的化学式中,书写正确的是( )
| A. | 氧化镁MgO2 | B. | 氯化铁FeCl2 | C. | 硝酸银AgNO3 | D. | 氢氧化铜CuOH |
13.下列各物质间的转化,能通过一步实现的是( )
①Cu→CuCl2 ②Fe(OH)3→FeCl3 ③SO2→Na2SO4 ④CH4→CO2 ⑤Ba(OH)2→NaOH ⑥CaO→Ca(OH)2.
①Cu→CuCl2 ②Fe(OH)3→FeCl3 ③SO2→Na2SO4 ④CH4→CO2 ⑤Ba(OH)2→NaOH ⑥CaO→Ca(OH)2.
| A. | ①②④⑤ | B. | ②④⑤⑥ | C. | ②③④⑤ | D. | ①②③⑤⑥ |
 蚊香是夏日驱除蚊虫的常用物品.丙烯菊酯(化学式C19H26O3)是蚊香中常含有的高效低毒杀虫剂.
蚊香是夏日驱除蚊虫的常用物品.丙烯菊酯(化学式C19H26O3)是蚊香中常含有的高效低毒杀虫剂.
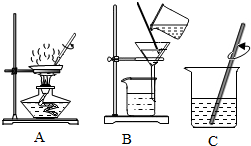
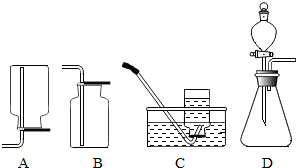 实验室制取气体的实验装置如图,请回答问题:
实验室制取气体的实验装置如图,请回答问题: