题目内容
15.A、B、C代表三种单质,甲、乙代表两种化合物,在一定条件下它们之间有如下关系:①A+C→甲; ②B+C→乙; ③A+乙→B+甲.请你根据初中化学学习过的常见物质知识回答下列问题:
(1)乙物质中的元素共有2种.
(2)如果常温下甲是无色、无味、无毒的气体,则A的化学式是CO,反应③的化学方程式可能为CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
(3)如果常温下甲是无色液体,则A的化学式是H2,反应③的化学方程式可能为H2 +CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
分析 根据A、B、C代表三种单质,甲、乙代表两种化合物,如果常温下甲是无色、无味、无毒的气体,①A+C→甲; ②B+C→乙; ③A+乙→B+甲,猜想A是碳,B是氧气,甲是二氧化碳,乙是一氧化碳,一氧化碳和氧化铜反应会生成铜和二氧化碳;如果常温下甲是无色液体,猜想甲是水,A是氢气,C是氧气,B是铜,乙是氧化铜,然后将猜想的物质进行验证即可.
解答 解:(1)根据质量守恒定律和B+C→乙,两种单质生成一种化合物,根据质量守恒定律,则可知乙物质中的元素共有2种;
(2)如果常温下甲是无色、无味、无毒的气体,①A+C→甲; ②B+C→乙; ③A+乙→B+甲,猜想A是碳,B是氧气,甲是二氧化碳,乙是一氧化碳,一氧化碳和氧化铜反应会生成铜和二氧化碳,碳和氧气点燃生成二氧化碳,铜和氧气加热生成氧化铜,氧化铜和一氧化碳加热生成铜和二氧化碳,猜想正确,所以A的化学式是CO,反应③的化学方程式可能为CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
(3)如果常温下甲是无色液体,猜想甲是水,A是氢气,C是氧气,B是铜,乙是氧化铜,氢气和氧气点燃生成水,铜和氧气加热生成氧化铜,氧化铜和氢气加热生成铜和水,猜想正确,所以A的化学式是H2,反应③的化学方程式可能为H2 +CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
故答案为:(1)2;
(2)CO,CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
(3)H2,H2 +CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 黄冈创优卷系列答案
黄冈创优卷系列答案| A. | 浓溶液一定是饱和溶液 | |
| B. | 浓硫酸溶解于水时会吸热 | |
| C. | 碘几乎不溶于水,但易溶于酒精 | |
| D. | 100g水中溶解了36gNaCl后达到了饱和,则该氯化钠溶液的质量分数为36% |
| A. | 水电解得到氢气和氧气,证明分子是可分的 | |
| B. | 水电解得到氢气和氧气,说明水中含有氢分子和氧分子 | |
| C. | 水电解时水分子发生了变化,不再保持水的化学性质 | |
| D. | 水电解的反应中,氢原子和氧原子都没有发生变化 |
| A. | CaCO3(Na2CO3) | B. | KCl(MnO2) | C. | NaCl(Na2CO3) | D. | Ag(Al) |
| A. | (1)(2)(3)(4) | B. | (1)(2)(3) | C. | (1)(2) | D. | (3)(4) |
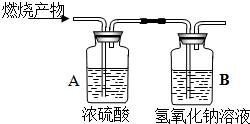 有一钢瓶气体,可能是H2、CO、CH4三种气体中的其中一种或几种的混合,现取少量气体在氧气中燃烧,并将生成的产物通入如图的装置.其中浓硫酸具有吸水性.
有一钢瓶气体,可能是H2、CO、CH4三种气体中的其中一种或几种的混合,现取少量气体在氧气中燃烧,并将生成的产物通入如图的装置.其中浓硫酸具有吸水性.