题目内容
5.一定质量的碳酸钙与200克质量分数为3.65%的稀盐酸恰好完全反应,求碳酸钙的质量.分析 由参加反应的盐酸的质量,由反应的化学方程式计算出碳酸钙的质量即可.
解答 解:设碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
x 200g×3.65%
$\frac{100}{x}=\frac{73}{200g×3.65%}$
x=10g
答:碳酸钙的质量为10g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
20.下列粒子结构示意图中,表示阳离子的是( )
| A. | 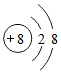 | B. |  | C. |  | D. | 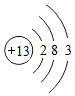 |
4.如图四个图象中能正确反映其对应实验操作的是( )
| A. |  表示向氢氧化钠溶液中加水稀释 | |
| B. |  表示将等质量的铁片和镁条分别与质量分数相同的足量的稀盐酸反应 | |
| C. |  表示等质量的石灰石块和石灰石粉分別与质量分数相同的足量的稀盐酸反应 | |
| D. |  表示用一氧化碳还原氧化铁 |
11.将ag锌粒加入一定质量的MgSO4、CuSO4和AgNO3的混合溶液中,充分反应后过滤,将滤渣洗涤、烘干后称量质量为bg,向滤液和滤渣中分别加入稀盐酸,下列有关现象和结论,不合理的是( )
| A. | 如果滤液中产生白色沉淀,则滤液的颜色为蓝色 | |
| B. | 滤渣的质量可能等于所加锌粒的质量 | |
| C. | 如果滤渣中有气体生成,则滤渣中一定含有4种金属 | |
| D. | 反应后所得滤液中至少含有两种金属离子 |
8.2016年“世界环境日”中国确定的主题为“改善环境质量,推动绿色发展”.下列做法与之相违背的是( )
| A. | 作物秸杆就地焚烧 | B. | 公共场所严禁吸烟 | ||
| C. | 积极使用降解塑料 | D. | 工业废水达标排放 |
9.下列变化中,属于化学变化的是( )
| A. | 铁水铸成锅 | B. | 车胎爆炸 | C. | 汽油挥发 | D. | 酿制美酒 |
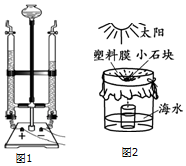 水是重要资源.
水是重要资源.