题目内容
 右图是配制好的硫酸钠溶液的标签,请根据标签上的文字信息,进行计算:
右图是配制好的硫酸钠溶液的标签,请根据标签上的文字信息,进行计算:
(1)硫酸钠中钠、硫元素的质量比是______;
(2)硫酸钠中钠元素的质量分数是______ (精确到0.1%);
(3)取氯化钡固体样品26g,放入烧杯中加水完全溶解并过滤,往滤液中滴加上述配制的硫酸钠溶液至完全反应,然后过滤、烘干.称得沉淀23.3g.计算:
①该样品中氯化钡的质量分数是多少?
②用去硫酸钠溶液的质量是多少g?
解:(1)硫酸钠中钠、硫元素的质量比是(23×2):32=23:16;?
(2)硫酸钠中钠元素的质量分数是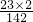 ×100%≈32.4%;
×100%≈32.4%;
(3)设样品中BaCl2的质量为x,反应用去Na2SO4溶液的质量为y.
BaCl2+Na2SO4═BaSO4↓+2NaCl
208 142 233
x y×10% 23.3g
 =
=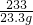 x=20.8g
x=20.8g
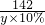 =
=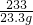 y=142g
y=142g
∴样品中BaCl2的质量分数为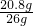 ×100%=80%
×100%=80%
答:样品中BaCl2的质量分数为80%,反应用去Na2SO4溶液的质量为142g;
故答案为:(1)23:16;(2)32.4%;(3)①80%;②142g.
分析:(1)元素的质量比=相对原子质量与相应原子个数的乘积比;
(2)某元素质量分数=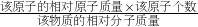 ×100%;
×100%;
(3)①利用氯化钡和硫酸钠反应的化学方程式,根据硫酸钡沉淀的质量求出氯化钡的质量,再根据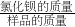 ×100%,求出样品中氯化钡的质量分数;
×100%,求出样品中氯化钡的质量分数;
②根据硫酸钡的质量求出硫酸钠的质量,再根据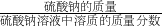 ×100%,求出所用的硫酸钠溶液的质量.
×100%,求出所用的硫酸钠溶液的质量.
点评:了解溶液中溶质的质量分数、物质中元素的质量分数、元素的质量比的计算方法,并要学会结合反应原理灵活运用解答问题.
(2)硫酸钠中钠元素的质量分数是
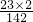 ×100%≈32.4%;
×100%≈32.4%;(3)设样品中BaCl2的质量为x,反应用去Na2SO4溶液的质量为y.
BaCl2+Na2SO4═BaSO4↓+2NaCl
208 142 233
x y×10% 23.3g
 =
=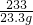 x=20.8g
x=20.8g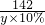 =
=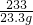 y=142g
y=142g∴样品中BaCl2的质量分数为
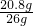 ×100%=80%
×100%=80%答:样品中BaCl2的质量分数为80%,反应用去Na2SO4溶液的质量为142g;
故答案为:(1)23:16;(2)32.4%;(3)①80%;②142g.
分析:(1)元素的质量比=相对原子质量与相应原子个数的乘积比;
(2)某元素质量分数=
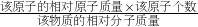 ×100%;
×100%;(3)①利用氯化钡和硫酸钠反应的化学方程式,根据硫酸钡沉淀的质量求出氯化钡的质量,再根据
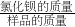 ×100%,求出样品中氯化钡的质量分数;
×100%,求出样品中氯化钡的质量分数;②根据硫酸钡的质量求出硫酸钠的质量,再根据
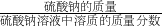 ×100%,求出所用的硫酸钠溶液的质量.
×100%,求出所用的硫酸钠溶液的质量.点评:了解溶液中溶质的质量分数、物质中元素的质量分数、元素的质量比的计算方法,并要学会结合反应原理灵活运用解答问题.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
右图是则配制好的硫酸钠溶液的标签,请根据标签上的文字信息,进行计算:
(1)该硫酸钠溶液中溶剂质量为 g;
(2)取氯化钡固体样品26g,放入烧杯中加水完全溶解并
过滤,往滤液中滴加上述配制的硫酸钠溶液至完全反应,
然后过滤、烘干。称得沉淀23.3g。计算:
①该样品中氯化钡的质量分数是多少?
②用去硫酸钠溶液的质量是多少g?
|
 右图是配制好的硫酸钠溶液的标签,请根据标签上的文字信息,进行计算:
右图是配制好的硫酸钠溶液的标签,请根据标签上的文字信息,进行计算: