题目内容
20. 如图是甲、乙两种物质的溶解度曲线.请回答:
如图是甲、乙两种物质的溶解度曲线.请回答:(1)当甲中混有少量乙时,可用降温结晶方法提纯甲.
(2)30℃时,若将5g甲物质放入10g水中充分溶解得到14g溶液.
(3)若B点表示60℃时将甲放入100g水中,将其变成恰好饱和的溶液的方法有:
①变成温度不变,需加入60g甲;
②变成浓度不变,降温到30℃.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)甲物质的溶解度受温度变化影响较大,所以当甲中混有少量乙时,可用降温结晶方法提纯甲;
(2)30℃时,甲物质的溶解度是40g,所以将5g甲物质放入10g水中充分溶解得到14g溶液;
(3)若B点表示60℃时将甲放入100g水中,溶质质量为40g,将其变成恰好饱和的溶液的方法有:
①60℃时,甲物质的溶解度是100g,所以变成温度不变,需加入60g甲;
②30℃时,甲物质的溶解度是40g,变成浓度不变,降温到30℃.
故答案为:(1)降温结晶;
(2)14;
(3)①60;
②30.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
1.下列现象不属于缓慢氧化的是( )
| A. | 塑料、橡胶制品的老化 | B. | 铁、铜等金属表面的锈蚀 | ||
| C. | 生物的呼吸作用 | D. | 燃放烟花爆竹 |
8.下列物质属于盐的是( )
| A. | 生石灰 | B. | 石灰石 | C. | 纯碱 | D. | 烧碱 |
5.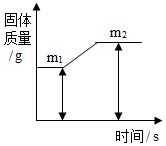 镁带在空气中完全燃烧后生成氧化镁,其固体物质变化可用图表示,则m1与m2质量差表示的质量是( )
镁带在空气中完全燃烧后生成氧化镁,其固体物质变化可用图表示,则m1与m2质量差表示的质量是( )
 镁带在空气中完全燃烧后生成氧化镁,其固体物质变化可用图表示,则m1与m2质量差表示的质量是( )
镁带在空气中完全燃烧后生成氧化镁,其固体物质变化可用图表示,则m1与m2质量差表示的质量是( )| A. | 生成氧化镁的质量 | B. | 参加反应镁的质量 | ||
| C. | 参加反应的氧气的质量 | D. | 多余氧气的质量 |
12.三种固体物质a、b、c的溶解度曲线如图所示,则下列说法不正确的是( )

| A. | t1℃时三种物质的饱和溶液中溶质的质量分数大小为b>a=c | |
| B. | a中混有少量b时可采取降温结晶的方法提纯得到a | |
| C. | t2℃时,将50g a物质加入到100g水中完全溶解形成饱和溶液 | |
| D. | a、b、c三种物质的饱和溶液从t2℃降温到t1℃时都有晶体析出 |
10.为了除去灯泡中可能混入的微量氧气,有些白炽灯在灯丝的支架上附着了少量的某种红色物质.该红色物质可能是( )
| A. | 红色油漆 | B. | 红磷 | C. | 红砖粉末 | D. | 高锰酸钾 |
 中和反应在工农业生产中应用广泛,现向40g 10%的氢氧化钠溶液中不断滴加盐酸,同时测定溶液pH的变化(曲线如图),
中和反应在工农业生产中应用广泛,现向40g 10%的氢氧化钠溶液中不断滴加盐酸,同时测定溶液pH的变化(曲线如图),