题目内容
6.小强同学在化学氧自救器的说明书中看到“人呼出气体中的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)接触能产生氧气后,对自救器内发生的化学反应原理产生了探究欲望.在老师指导下,小强与同学们展开了以下两个实验探究活动,请你参与.活动Ⅰ:用图甲所示的由a、b、c、d组合成的成套装置和有关药品制取并收集氧气.

(1)化石燃料之一的煤燃烧生成二氧化碳的方程式为C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;实验室通常用石灰石与稀盐酸制取二氧化碳,则a装置可采用如图乙中的③(填序号),有关反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)c装置的作用是c装置中的氢氧化钠溶液吸收未与超氧化钾反应的二氧化碳.
(3)用排水法法收集氧气,该收集方法是根据氧气不易溶于水的性质而确定的.证明生成的气体是氧气,使用带火星的木条进行检验.
活动Ⅱ:探究二氧化碳与超氧化钾反应除生成氧气外,还生成其它什么物质?
[老师提示]二氧化碳与超氧化钾反应的生成物只有两种,其一是氧气,其二是一种化合物.
[作出猜想]二氧化碳与超氧化钾反应生成的化合物到底是哪种物质?小强作出了以下三种猜想:
①是一种酸; ②是一种碱; ③是一种碳酸盐.
通过对反应物有关的元素组成的分析,小影同学认为猜想①、②(填序号)一定是错误的,理由是化学反应前后元素的种类不变,反应物的组成中无氢元素故无酸碱生成.
[进行实验]同学们通过以下实验验证小强同学的另一个猜想.
| 实验步骤 | 实验现象 | 实验结论 |
| 将二氧化碳与超氧化钾反应后的固体加入试管中,倒入稀盐酸,将产生的气体导入石灰水 | 固体逐渐溶解有气泡产生,石灰水变浑浊 | 二氧化碳与超氧化钾反应生成的化合物是碳酸钾(填名称). |
分析 (1)煤的主要成分是碳,发生装置主要由反应物的状态和反应条件决定;
(2)根据二氧化碳与氢氧化钠反应分析;
(3)收集装置主要由气体的密度和溶水性决定;氧气具有助燃性,所以检验氧气的存在采用带火星的木条;
活动Ⅱ:[作出猜想]
要推断二氧化碳和超氧化钾反应的产物可根据质量守恒定律进行分析判断;
[进行实验]
可根据二氧化碳和超氧化钾反应的生成物---碳酸钾的性质(碳酸钾可与酸反应生成二氧化碳)进行实验设计;
[交流与讨论]
(1)根据二氧化碳和超氧化钾反应的反应物、生成物及方程式的书写方法书写方程式;
解答 解:(1)煤的主要成分是碳,碳与氧气反应生成二氧化碳,化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;反应物的状态是固态和液态,反应条件是常温,应选固-液不加热型的发生装置,装置②长颈漏斗下端没有伸到液面以下,所以选③;石灰石的主要成份是碳酸钙,盐酸的溶质是氯化氢气体,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳;
(2)用c装置中的氢氧化钠溶液吸收未与超氧化钾反应的二氧化碳.
(3)氧气不易溶于水,可用排水法收集,氧气的密度比空气大,可以用向上排空气法收集,氧气具有助燃性,可以用带火星的木条检验其存在;
活动Ⅱ:[作出猜想]
根据质量守恒定律,化学反应前后元素的种类不变;反应前物质中含钾、碳、氧三种元素,由于反应物中无H元素,而酸和碱中都含有氢元素,所以不可能为酸和碱;
[进行实验]
小强同学的另一个猜想是生成碳酸盐,而碳酸盐的特点是可以与酸反应生成使澄清石灰水变浑浊的气体,故可向样品中加入稀盐酸并将生成气体通入澄清的石灰水进行鉴定;
[交流与讨论]
(1)二氧化碳与超氧化钾反应的产物K2CO3和O2,方程式是4KO2+2CO2=2K2CO3+3O2;
故答案为:(1)C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;③;CaCO3+2HCl═CaCl2+H2O+CO2↑
(2)c装置中的氢氧化钠溶液吸收未与超氧化钾反应的二氧化碳
(3)排水法(向上排空气法)、不易溶于水(密度比空气大)、带火星的木条
【作出猜想】:①、②;化学反应前后元素的种类不变,反应物的组成中无氢元素故无酸碱生成.
【进行实验】:试管中,倒入稀盐酸,将产生的气体导入石灰水.
固体逐渐溶解有气泡产生,石灰水变浑浊.碳酸钾
4KO2+2CO2=2K2CO3+3O2
点评 此题综合考察了物质的制取与收集装置的选取,物质的推断、鉴定,化学方程式的书写、质量守恒定律的运用等等,需要综合掌握化学知识,大胆的合理的进行推理.

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案| A. | 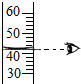 液体体积读数 | B. |  熄灭酒精灯 | C. | 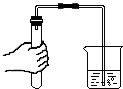 检查气密性 | D. | 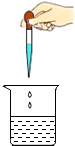 滴加液体 |
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | Na2SO4(NaOH) | 稀硫酸 | 加过量的稀硫酸、蒸发结晶 |
| B | NaC1(Na2CO3) | CaC12溶液 | 加入适量的CaC12溶液,过滤、将滤渣洗涤、干燥 |
| C | KC1(KC1O3) | MnO2 | 加MnO2,加热后冷却 |
| D | H2 (CO2) | 氢氧化钠溶液、浓硫酸 | 将混合气体先通过足量的氢氧化钠溶液的洗气瓶,再通过浓硫酸的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 原干燥剂中氧化钙的质量为5.6g | |
| B. | 使用过的干燥剂中可能含有氧化钙、氢氧化钙、碳酸钙等物质 | |
| C. | 反应后溶液中溶质的质量为11.1g | |
| D. | 反应后溶液的质量为105.6g |
| A. | 耐腐蚀性 | B. | 导电性 | C. | 导热性 | D. | 延展性 |
| A. | Na+ | B. | Cl- | C. | H2O | D. | 以上三种 |
| A. | 水由氢元素和氧元素组成 | |
| B. | 花香四溢说明分子间有间隔 | |
| C. | 向氢氧化钙溶液中滴入几滴无色酚酞试液,溶液变成红色 | |
| D. | 用灼烧的方法鉴别羊毛和涤纶 |