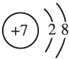题目内容
将5克某物质分别放入95克水中溶解后,所得溶液中溶液质量分数最大的是( )
| A、KNO3 |
| B、CaO |
| C、SO3 |
| D、CuSO4?7H20 |
考点:溶质的质量分数
专题:溶液、浊液与溶解度
分析:四种物质溶于水后,其中硝酸钾形成硝酸钾溶液,氧化钙与水反应生成氢氧化钙溶液,三氧化硫与水反应生成硫酸溶液,7水硫酸铜形成硫酸铜溶液;由于是充分溶解,则硝酸钾、硫酸铜、硫酸溶液质量都为100g不变;根据反应方程式分别计算出氢氧化钙、硫酸溶质、硫酸铜的质量;而氢氧化钙的溶解度很小,故溶质的质量分数远远的要比10%小;最后比较剩余三种溶液中溶质质量最大的则是溶质质量分数最大的.
解答:解:
A、5g硝酸钾充分溶解在95g水中,硝酸钾溶质的质量为5g;则硝酸钾溶液的溶质质量分数为:
×100%=5%;
B、5氧化钙充分溶解在95g水中,则设生成氢氧化钙的质量为x,
CaO+H2O═Ca(OH)2
56 74
5g x
=
x=6.6g
则氢氧化钙溶液中溶质的质量为13.2g;
虽然生成的13.2g氢氧化钙,但是Ca(OH)2微溶于水(<0.1g),所以溶质质量分数要远远的小于5%;
C、5g三氧化硫充分溶解在95g水中,则设生成硫酸的质量为y;
SO3+H2O═H2SO4
80 98
5g y
=
解得:y=6.125g;
则硫酸溶液的溶质质量分数:
×100%=6.125%;
D、5g7水硫酸铜中硫酸铜的质量=5g×
×100%≈2.9g
则硫酸铜溶液的溶质质量分数:
×100%=2.9%
答案:C
A、5g硝酸钾充分溶解在95g水中,硝酸钾溶质的质量为5g;则硝酸钾溶液的溶质质量分数为:
| 5g |
| 5g+95g |
B、5氧化钙充分溶解在95g水中,则设生成氢氧化钙的质量为x,
CaO+H2O═Ca(OH)2
56 74
5g x
| 56 |
| 5g |
| 74 |
| x |
x=6.6g
则氢氧化钙溶液中溶质的质量为13.2g;
虽然生成的13.2g氢氧化钙,但是Ca(OH)2微溶于水(<0.1g),所以溶质质量分数要远远的小于5%;
C、5g三氧化硫充分溶解在95g水中,则设生成硫酸的质量为y;
SO3+H2O═H2SO4
80 98
5g y
| 80 |
| 5g |
| 98 |
| y |
解得:y=6.125g;
则硫酸溶液的溶质质量分数:
| 6.125g |
| 5g+95g |
D、5g7水硫酸铜中硫酸铜的质量=5g×
| 160 |
| 160+126 |
则硫酸铜溶液的溶质质量分数:
| 2.9g |
| 5g+95g |
答案:C
点评:此题是对溶质质量分数的考查,解题关键点是考虑10g物质放入水中时是否发生了变化,溶质的量是否发生了改变.

练习册系列答案
相关题目
化学反应前后,下列诸项中肯定没有变化的是( )
①原子的数目; ②元素的化合价; ③元素的种类; ④物质的总质量;⑤物质的种类;⑥原子的种类.
①原子的数目; ②元素的化合价; ③元素的种类; ④物质的总质量;⑤物质的种类;⑥原子的种类.
| A、①③④⑤⑥ | B、①③⑤ |
| C、①②④⑥ | D、①③④⑥ |
下列对分子、原子的有关叙述,错误的是( )
| A、分子在化学反应前后种类不变 |
| B、原子在化学反应前后种类不变 |
| C、原子在化学反应前后总数不变 |
| D、原子是化学反应中的最小微粒 |
下列说法正确的是( )
| A、空气中氮气的质量分数为78%,氧气的质量分数为21% |
| B、因为氧气能支持燃烧,所以可用作燃料 |
| C、氮气用作保护气,反映氮气的化学性质不活泼 |
| D、二氧化碳是一种大气污染物 |
4岁的小英耳朵有点痛,需要服用扑热息痛糖浆或滴剂(糖浆与滴剂的作用相同),而家里只有扑热息痛滴剂.对于一个4岁的儿童来说,服用糖浆的安全用量为6毫升(如图).则服用多少毫升的滴剂等于服用了6毫升用量的糖浆( )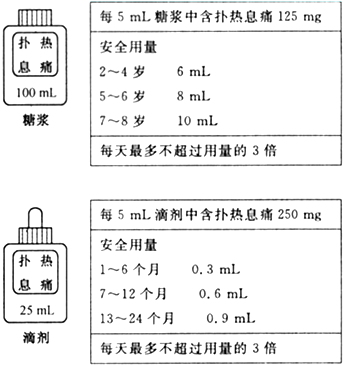

| A、3毫升 | B、6毫升 |
| C、9毫升 | D、12毫升 |
下列有关粒子的说法中,正确的是( )
| A、最外层电子数相同的粒子化学性质一定相同 |
| B、质子数小于核外电子数的粒子是阳离子 |
| C、原子中一定都含有质子、中子和电子 |
| D、分子、原子、离子都可以直接构成物质 |
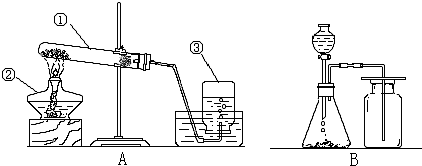
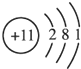
 下列示意图表示的粒子与氮元素具有相似化学性质的是( )
下列示意图表示的粒子与氮元素具有相似化学性质的是( )