题目内容
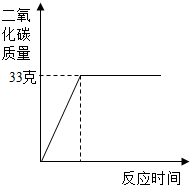
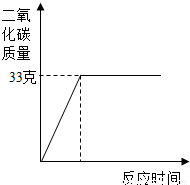
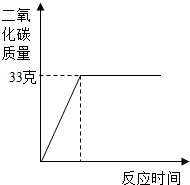 我省巢湖市石灰石资源丰富.滨湖中学化学兴趣小组计划研究繁昌一石灰石矿山的碳酸钙含量.它们选取了100克石灰石样品,在其中加入足量的稀盐酸,测得生成的二氧化碳质量与反应时间的关系如图所示.请你分析并计算后回答:
我省巢湖市石灰石资源丰富.滨湖中学化学兴趣小组计划研究繁昌一石灰石矿山的碳酸钙含量.它们选取了100克石灰石样品,在其中加入足量的稀盐酸,测得生成的二氧化碳质量与反应时间的关系如图所示.请你分析并计算后回答:(1)反应生成的二氧化碳质量为
(2)此石灰石样品中碳酸钙的质量分数是多少?
分析:(1)由图可知生成二氧化碳的质量.
(2)由二氧化碳和样品的质量根据碳酸钙与稀盐酸反应的化学方程式可以计算出样品中碳酸钙的质量分数.
(2)由二氧化碳和样品的质量根据碳酸钙与稀盐酸反应的化学方程式可以计算出样品中碳酸钙的质量分数.
解答:解:(1)由图中曲线可知生成二氧化碳的质量为33g.
(2)设样品中碳酸钙的质量分数为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
100g×x 33g
=
,x=75%
答:(1)33;
(2)此石灰石样品中碳酸钙的质量分数为75%.
(2)设样品中碳酸钙的质量分数为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
100g×x 33g
| 100 |
| 44 |
| 100g×x |
| 33g |
答:(1)33;
(2)此石灰石样品中碳酸钙的质量分数为75%.
点评:本题主要考查含杂质物质的化学方程式计算,难度较大.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
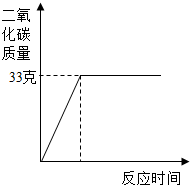 我省巢湖市石灰石资源丰富.滨湖中学化学兴趣小组计划研究繁昌一石灰石矿山的碳酸钙含量.它们选取了100克石灰石样品,在其中加入足量的稀盐酸,测得生成的二氧化碳质量与反应时间的关系如图所示.请你分析并计算后回答:
我省巢湖市石灰石资源丰富.滨湖中学化学兴趣小组计划研究繁昌一石灰石矿山的碳酸钙含量.它们选取了100克石灰石样品,在其中加入足量的稀盐酸,测得生成的二氧化碳质量与反应时间的关系如图所示.请你分析并计算后回答: