题目内容
6.某同学用同规格且光亮洁净无锈的铁钉进行了如图所示实验.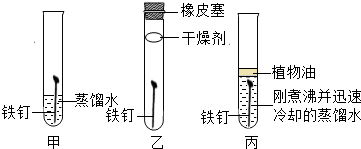
(1)一段时间后,铁钉表面生锈的是甲(填“甲”、“乙”或“丙”);铁制品生锈的条件是与H2O、O2(填化学式)接触.
(2)实验丙中要用“刚煮沸并迅速冷却的蒸馏水”的目的是除去水中溶解的氧气,使铁不能与氧气接触.
(3)工业上常用盐酸除锈,其反应的化学方程式为Fe2O3 +6HCl=2FeCl3+3H2O.
分析 (1)铁生锈的条件是:与氧气接触,有水参加;
(2)刚煮沸蒸馏水中没有氧气;
(3)根据铁锈的主要成分氧化铁与盐酸反应原理解答
解答 解:
(1)甲中铁钉与空气和水共同接触,乙中没有水,丙中没有氧气,故甲表面生锈,铁生锈的条件是:与氧气接触,有水参加,二者缺一不可;
(2)实验丙中用“刚煮沸并迅速冷却的蒸馏水”是为了除去水中溶解的氧气,使铁不能与氧气接触,故答案为:除去水中溶解的氧气,使铁不能与氧气接触;
(3)氧化铁与盐酸反应生成氯化铁和水,化学方程式为:Fe2O3 +6HCl=2FeCl3+3H2O,故答案为:Fe2O3 +6HCl=2FeCl3+3H2O.
答案:
(1)甲 H2O、O2
(2)除去水中溶解的氧气,使铁不能与氧气接触;
(3)Fe2O3 +6HCl=2FeCl3+3H2O
点评 本题考查的是铁锈以及铁与盐酸反应的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
17.下列实验现象的描述中,不正确的是( )
| A. | 细铁丝在氧气中燃烧,火星四射,产生黑色固体 | |
| B. | 将氢氧化钠溶液滴入氯化铁溶液中,有红褐色沉淀产生 | |
| C. | 将二氧化碳通入紫色石蕊溶液中,溶液变为蓝色 | |
| D. | 将(NH4)2SO4和熟石灰混合研磨,有刺激性气味产生 |
14.下列有关概念的辨析中正确的是( )
| A. | 一种元素只能组成一种单质 | |
| B. | 原子不能保持物质的化学性质 | |
| C. | 带有电荷的微粒可能不是离子 | |
| D. | 元素的种类是由原子的最外层电子数决定的 |
1.下列4个图象能正确反映对应变化关系是( )
| A. |  向一定量稀H2SO4中加入NaOH溶液 | |
| B. | 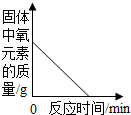 用酒精灯加热一定量KMnO4体 | |
| C. | 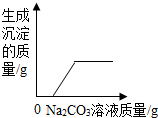 向一定量澄清石灰水中加入Na2CO3溶液 | |
| D. |  向盛有MnO2的烧杯中加入H2O2溶液 |
18. 如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )
如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )
 如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )
如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )| A. | 葡萄汁能使紫色石蕊试液变蓝 | B. | 施用草木灰可以降低土壤碱性 | ||
| C. | 鸡蛋清的碱性比牙膏强 | D. | 胃酸过多的人不宜多食泡菜 |
15.下列变化属于物理变化的是( )
| A. | 氨水挥发 | B. | 铁锅生锈 | C. | 碳铵分解 | D. | 油米霉变 |
16.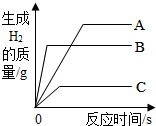 将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )(已知:A、B、C在生成物中均为+2价)
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )(已知:A、B、C在生成物中均为+2价)
 将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )(已知:A、B、C在生成物中均为+2价)
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是( )(已知:A、B、C在生成物中均为+2价)| A. | 消耗盐酸的质量是A>B>C | B. | 金属活动性顺序是A>B>C | ||
| C. | 反应速率由快到慢A>B>C | D. | 相对原子质量是A>B>C |
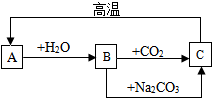 A、B、C是三种常见的含钙化合物,它们之间有如图所示的转化关系(部分产物略去)
A、B、C是三种常见的含钙化合物,它们之间有如图所示的转化关系(部分产物略去)