题目内容
19.t℃时,分别向盛有40ml水的烧杯中加入等质量的甲、乙两种可溶性的固体物质,使其充分溶解,可观察到如图Ⅰ所示的现象.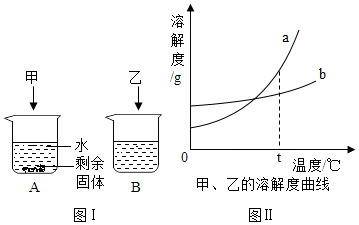
(1)t℃时,A(填“A”或“B”)烧杯中的溶液一定是饱和溶液.
(2)图Ⅱ中可表示甲物质的溶解度曲线的是b(填“a”或“b”).要使A烧杯中剩余的固体继续溶解可用升高温度或增加溶剂的方法.
分析 (1)根据溶液中有未溶解的固体溶质的溶液为不能再溶解该溶质的饱和溶液,进行分析解答.
(2)根据t℃甲、乙物质的溶解现象判断两物质的溶解度曲线,根据曲线表现出来的溶解度与温度变化关系,选择把甲物质继续溶解的方法.
解答 解:(1)t℃时,分别向盛有40ml水的烧杯中加入等质量的甲、乙两种可溶性的固体物质,甲物质有剩余,没有全部溶解,说明此时甲的溶液为饱和溶液.
(2)t℃40g水中溶解的乙物质比甲物质多,说明此时物质乙的溶解度比物质甲大,则a曲线表示的是乙,b曲线表示的是甲.
由于甲的溶解度随着温度的升高而增大,故可通过升温或增加水的方法把未溶解的甲物质溶解.
故答案为:(1)A;(2)b;升高温度或增加溶剂.
点评 本题难度不是很大,主要考查了固体溶解度曲线所表示的意义,掌握固体溶解度曲线的含义、饱和溶液的特征等是正确解答本题的关键.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
10.用“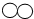 ”和“
”和“ ”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示.下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示.下列说法正确的是( )
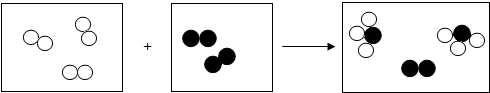
 ”和“
”和“ ”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示.下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示.下列说法正确的是( )
| A. | 在反应过程中A2和B2分子保持不变 | |
| B. | 该反应若A2的相对分子质量为m,B的相对原子质量为n,则X的相对分子质量为m+2n | |
| C. | 参加反应的A2、B2与X的微粒个数比为3:1:2 | |
| D. | 物质X含4种元素 |
14.欲将含少量盐酸的氯化钙溶液变为中性,在不用指示剂的条件下,应加入的试剂是( )
| A. | 石灰石 | B. | 生石灰 | C. | 氢氧化钠 | D. | 熟石灰 |
7.现有仪器:①试管、②锥形瓶、③广口瓶、④烧杯、⑤量筒、⑥集气瓶、⑦细口瓶,其中能作为反应容器的是( )
| A. | 除⑤外均可 | B. | 除⑤⑦外均可 | C. | 都可以 | D. | 除⑤⑥⑦外均可 |
4.下列实验现象的描述中,正确的是( )
| A. | 木炭在氧气中燃烧,生成有刺激性气味的气体 | |
| B. | 硫在氧气中燃烧,发出淡蓝色火焰 | |
| C. | 红磷在空气中燃烧产生大量的白雾 | |
| D. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 |
5.关于乙烯气(C2H4)燃烧C2H4+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2H2O的反应认识正确的是( )
| A. | 反应物与生成物的质量比为1:3:2:2 | |
| B. | 1个乙稀气和3个氧气在点燃条件下,生成2个二氧化碳和2个水 | |
| C. | 在常温和氧气混合就可以发生反应 | |
| D. | 参加反应的乙烯气中所含碳元素的质量等于生成二氧化碳中所含碳元素质量 |